马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
在广泛期小细胞肺癌(ED-SCLC)一线治疗中,PD-L1抑制剂(阿替利珠单抗、度伐利尤单抗)联合含铂化疗可以带来生存获益;后线治疗中,帕博利珠单抗、纳武利尤单抗±伊匹单抗同样具有一定疗效。
初诊时,约30%为局限期小细胞肺癌(LD-SCLC),不过预后仍差,中位OS为16-24 个月,5 年生存率仅为 25-33%。含铂双药化疗联合放疗是局限期小细胞肺癌的标准治疗,其中同步放化疗优于序贯放化疗,放疗在化疗第一个或第二个化疗结束后加入更优;另外,低剂量、每日两次及高剂量放疗,疗效未见明显差异;脑预防照射(PCI)可使3年的OS提高5.4%。
CheckMate 032研究(I/II期,单臂、小样本)为免疫后线治疗ED-SCLC,4周期纳武单抗±伊匹单抗,随后纳武单抗维持治疗,结果显示双免组优于单免组(ORR21.9% vs 11.6%),安全性可耐受。基于这些研究,设计了CheckMate 451(ED-SCLC)和STIMULI研究(LD-SCLC),探讨了“纳武单抗+伊匹单抗”在小细胞肺癌患者维持治疗中的有效性和安全性。今天我们分享《Ann Oncol》发表的STIMULI研究结果。
研究方法
STIMULI研究:是一项开放标签、随机、多中心、II 期试验,评估了局限期小细胞肺癌在标准“放化疗和PCI治疗”后±“纳武单抗和伊匹单抗”维持治疗的有效性和安全性。研究纳入I-IIIB 期,并且组织学或细胞学证实的局限期小细胞肺癌患者,ECOG评分为 0-1分,有足够的脏器功能,排除既往有系统性抗肿瘤治疗或胸部放疗史。患者在接受4周期化疗、以及85%PTV(planning target volume)胸部放疗和PCI治疗后,疾病未出现进展,之后随机分为免疫双药维持组和临床观察组。
治疗方案:1. 四周期含铂双药化疗(顺铂 25mg/m2第1、2、3天 或 顺铂 75mg/m2第1天 或 卡铂 AUC 5-6 第1天 + 依托泊苷 100mg/m2 第1、2、3天,q3w)。2. 同步放疗(45Gy/30天,1.5Gy bid 或 56Gy/28天,2Gy qd),在第一个或第二个化疗结束后加入;PCI(25Gy,10次)。3. 纳武单抗(1mg/kg)+ 伊匹单抗(3mg/kg),每21天重复×4周期,随后给予纳武单抗维持治疗(240mg、q2w),最多1年。
研究终点:主要研究终点为PFS,次要终点为OS、ORR、中位至治疗失败时间(TTF)及安全性。
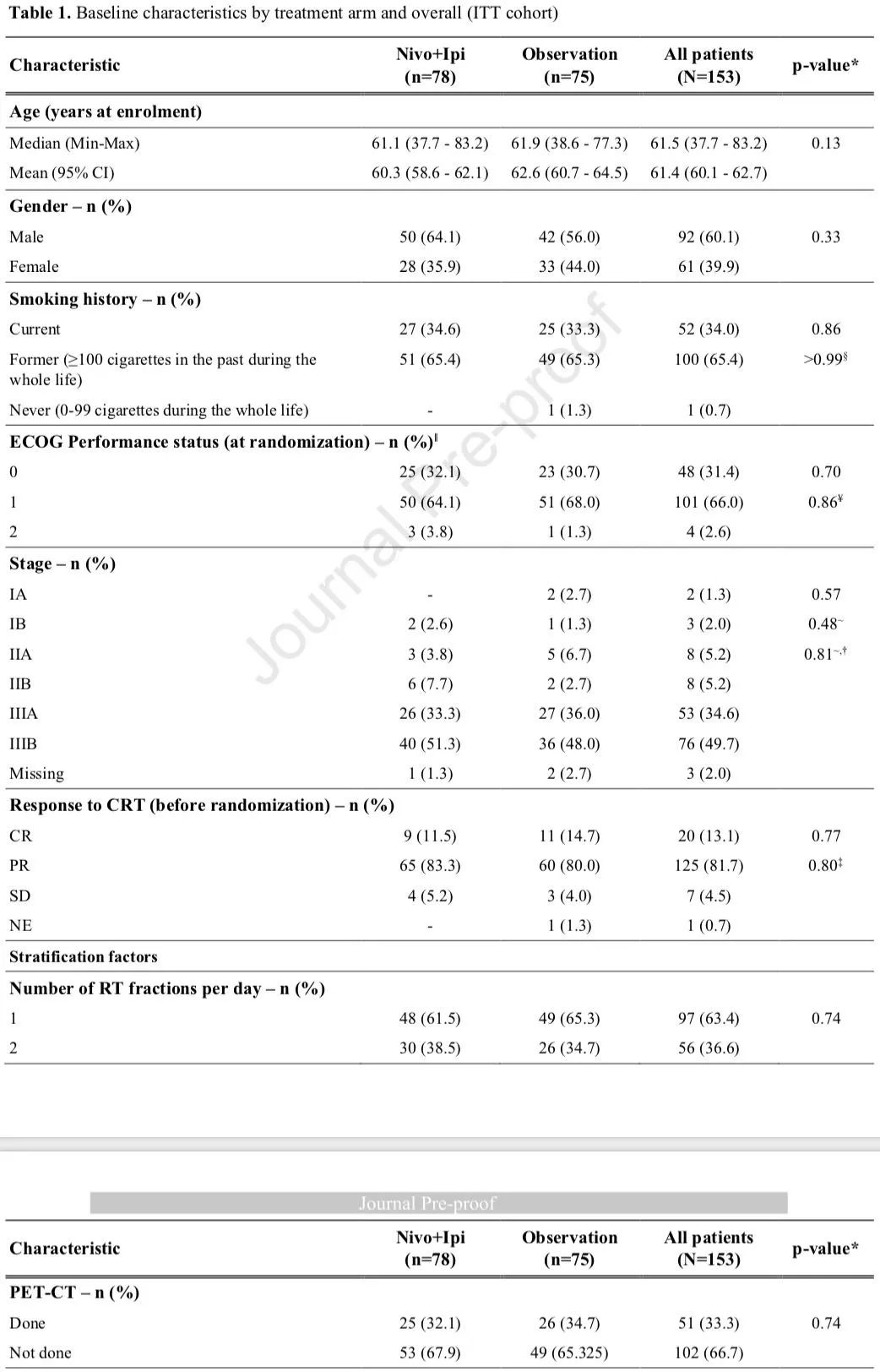
研究结果患者特征2015年12月至2019年4月,总共153名患者被随机分配到实验组和观察组,两组患者基线特征均衡可比。多数为男性、PS为1分、IIIB期。在诱导治疗阶段,同步放化疗的疗效评价为CR、PR、SD分别为13.1%、81.7%、4.5%。
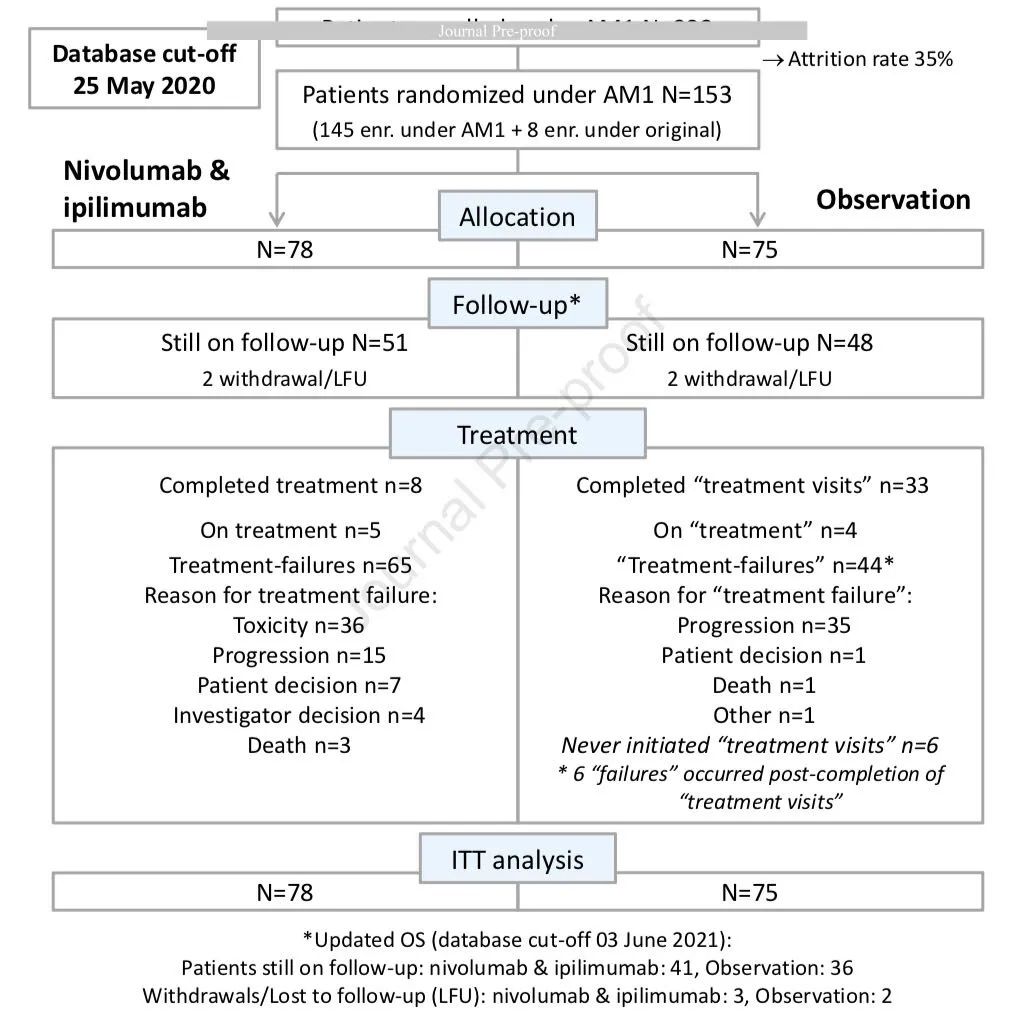
研究设计↑
患者基线特征→
临床疗效数据截止日期为 2020 年 5 月 25 日,中位随访时间为 22.4个月。实验组有65名患者停止治疗,其中36 名(55%)因为安全性,最常见不良反应为肺炎(10/36)。观察组有44名停止治疗,80%因为疾病进展。中位PFS:实验组(双免维持)、观察组分别为10.7个月 vs 14.5个月,无显著差异(HR=1.02;95%CI:0.66-1.58;P=0.93)。12个月的PFS率分别为48.1% vs 52.8%,24个月的PFS率分别43.2% vs 40.3%。
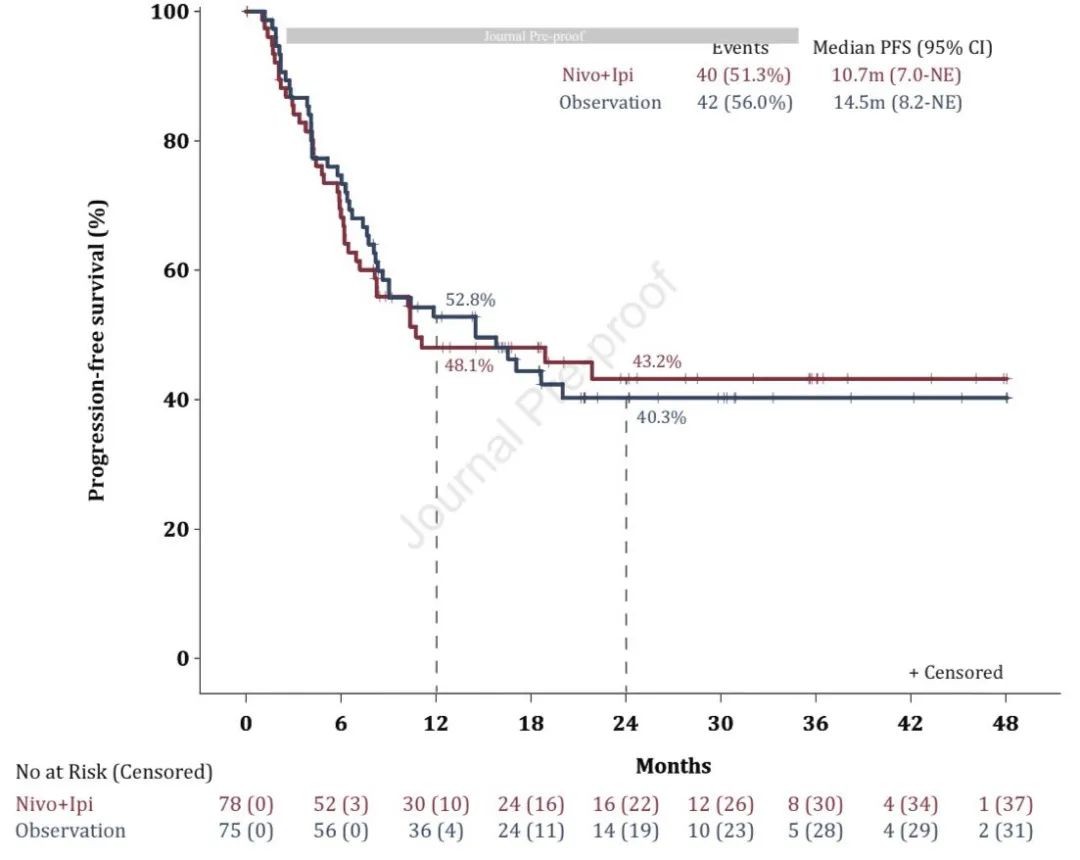
PFS
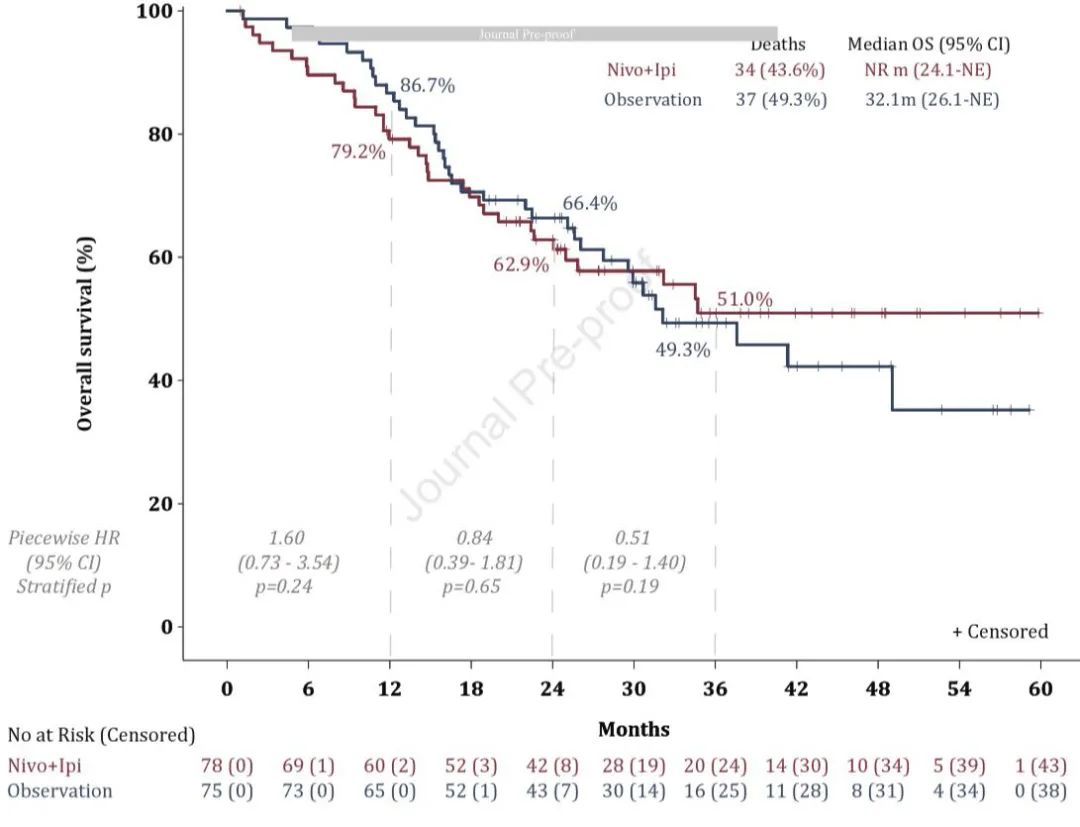
OS
中位OS:最新更新截止2021年6月3日,中位随访时间为 35.0 个月,实验组(双免维持)、观察组分别为未达到(NR) vs 32.1个月,无显著差异(HR=0.95;95%CI:0.59-1.52;P=0.82)。24 个月的OS 率分别为 62.9% vs 66.4%。ORR:实验组(双免维持)、观察组分别为38% vs 47%,统计无差异;两组的中位 DoR 均未达到,12 个月的 DoR 分别为 63.0% vs 73.2%。进展部位:大多数为新发转移灶,实验组(双免维持)、观察组分别为92%和77%;局部进展分别为15%和18%。出现1个转移部位分别为81%和70%;2个转移部位为16%和27%;3个转移部位均为3%。最常见转移部位是肝脏、淋巴结、肺部、脑部等。安全性实验组(双免维持)、观察组出现任何级别的不良反应为98.7% vs 86.7%,其中实验组治疗相关不良反应(TRAE)为96.2%。3级以上不良反应发生率为61.5% vs 25.3%,实验组中55.1%患者因TRAE终止治疗,并有5.1%的患者出现死亡,而观察组为1.3%。最常见的不良反应是疲劳和厌食。
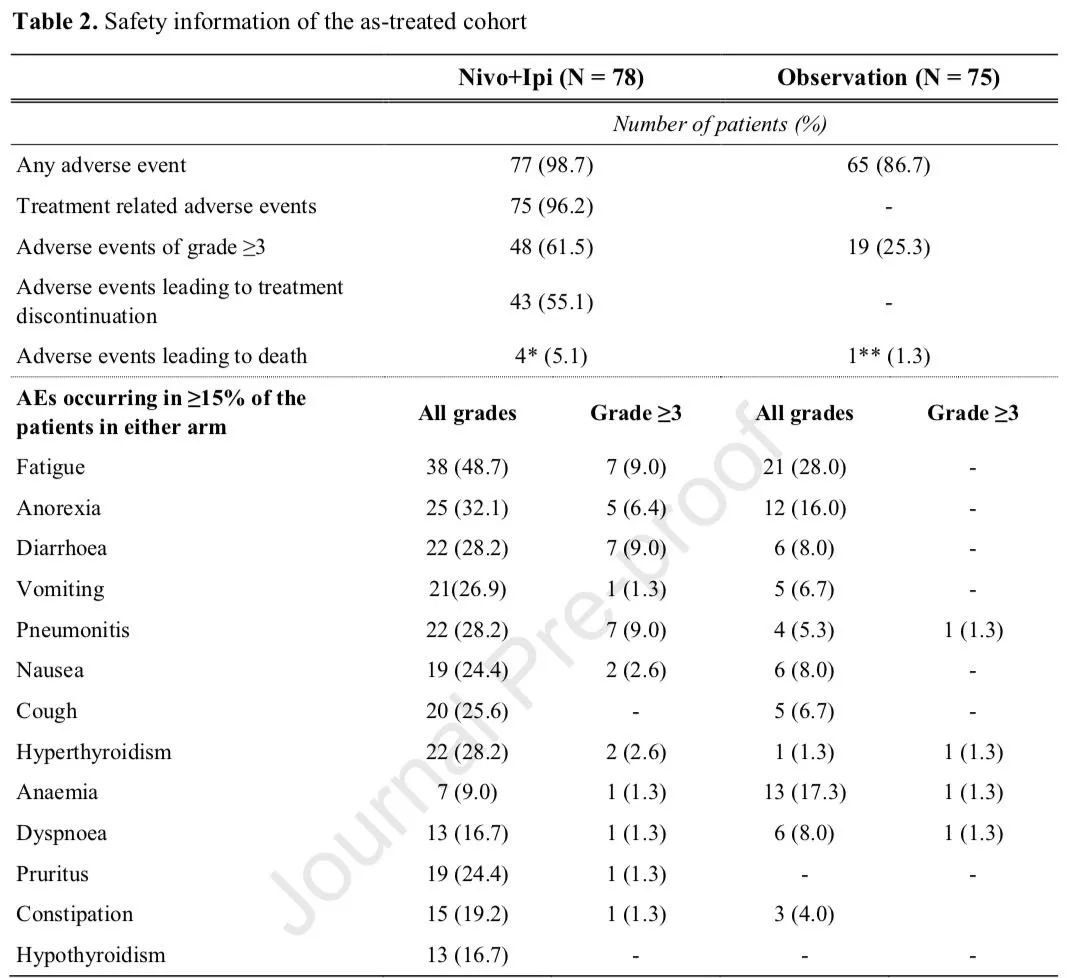
安全性
小 结
STIMULI 试验未达到其主要终点,即在LD-SCLC中放化疗后使用双免维持治疗未能改善 PFS。较高比例的治疗相关毒性以及终止治疗可能影响了疗效。
参考文献
Peters S, Pujol JL, Dafni U, et al. Consolidation nivolumab and ipilimumab versus observation in limited-disease small-cell lung cancer after chemo-radiotherapy - results from the randomised phase II ETOP/IFCT 4-12 STIMULI trial. Ann Oncol. 2021 Sep 23:S0923-7534(21)04490-2. doi: 10.1016/j.annonc.2021.09.011.
|