马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
Vivian 微 lin 肺癌前沿

在一些癌症患者中,检查点阻滞和过继性T细胞转移等免疫疗法的成功取得有限的成功,仍然有大部分患者对此类治疗无应答。多种机制参与肿瘤免疫逃避机制,尚缺乏有效的模型来预测个体患者是否以及如何应答。 Cell 发表的一项Proof-of-principle study研究显示,患者特异性上皮肿瘤类器官 patient specific epithelial tumor organoids可以刺激同一患者的外周血中产生肿瘤特异性T细胞,这为个体肿瘤对T细胞介导的抗肿瘤效应的敏感性机制研究打开了大门。

类器官是细胞衍生的体外3D器官模型,并允许在模拟内源性细胞组织和器官结构的环境中研究生物信息,例如细胞行为,组织修复和对药物或突变的反应。
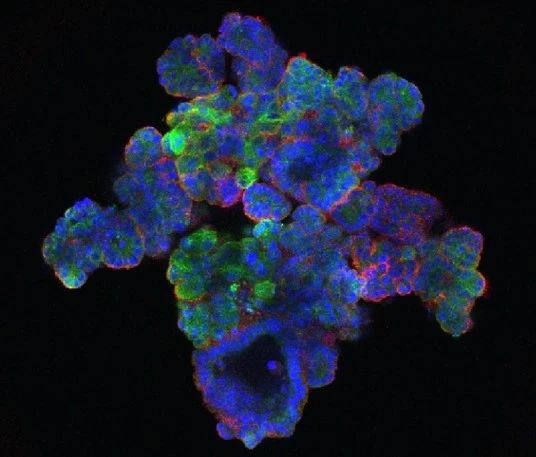
作者研究团队用错配修复缺陷的结直肠癌,(其具有高突变负荷和对检查点阻滞治疗的应答率较高)。从切除标本或粗 针活检组织培养肿瘤类器官,成功率为~60%,从而成功获得来自13名患者的15个肿瘤类器官 tumor organoids(其中8名患者的9个类器官是MHC class I proficient)。肿瘤类器官在形态学和遗传学方面反映了其来源的原始肿瘤。
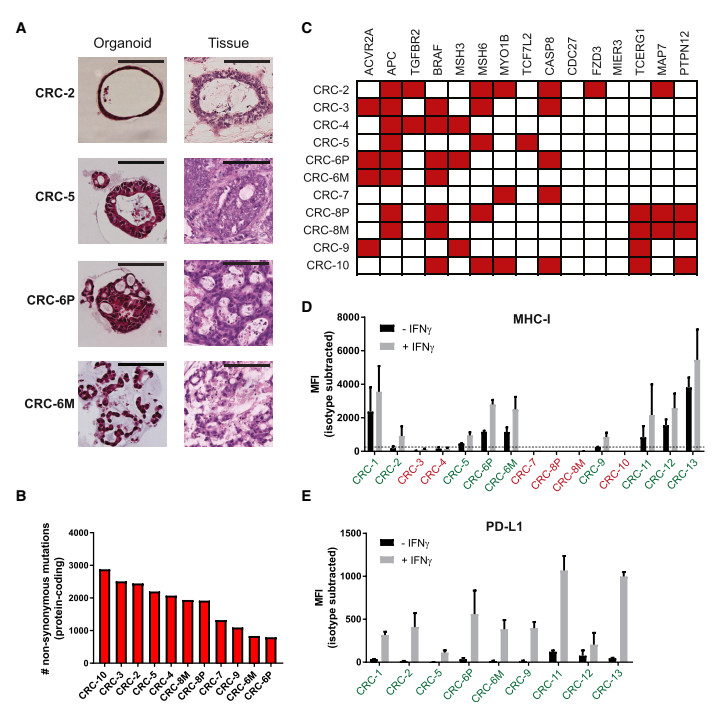
Characterization of a Panel of dMMR CRC Organoids
MHC class I proficient肿瘤类器官用IFNγ预刺激(以增加抗原呈递)并与程序性细胞死亡1(PD1)特异性抗体一起培养(以阻断来自肿瘤表达程序的抑制信号)细胞死亡1配体1(PDL1)),CD28特异性抗体(提供T细胞共刺激)和IL-2(支持T细胞增殖)。在这些条件下,8个类器官中的4个(50%)激活了来自同一患者的外周血单核细胞的CD8 + T细胞。对于由6名患有非小细胞肺癌的患者培养出的类器官获得了类似的结果。
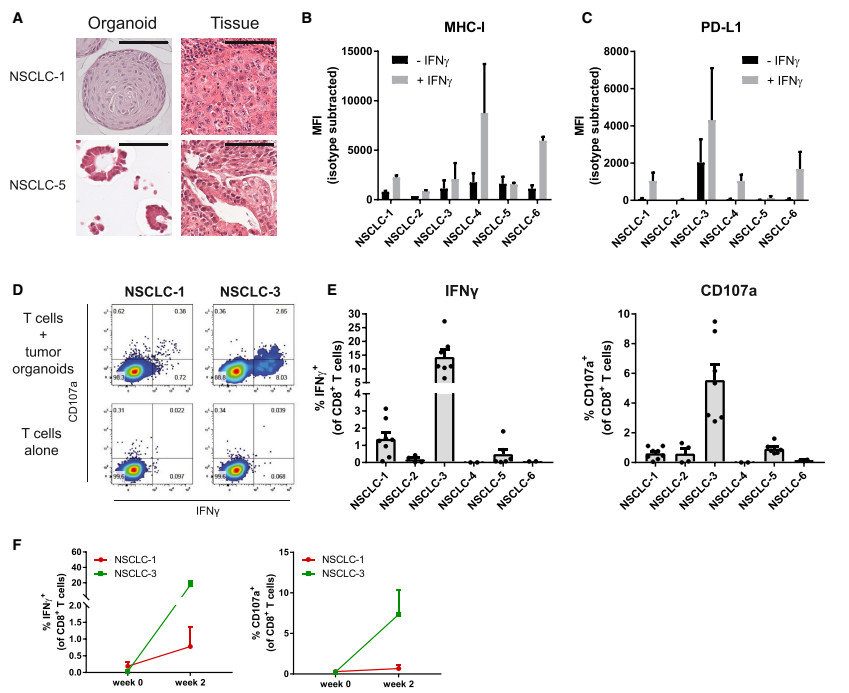
在4个病例中的3个中,活化的CD8 + T细胞的反应性对于培养的肿瘤类器官是特异性的,并且没有观察到针对自体健康组织类器官的反应性。
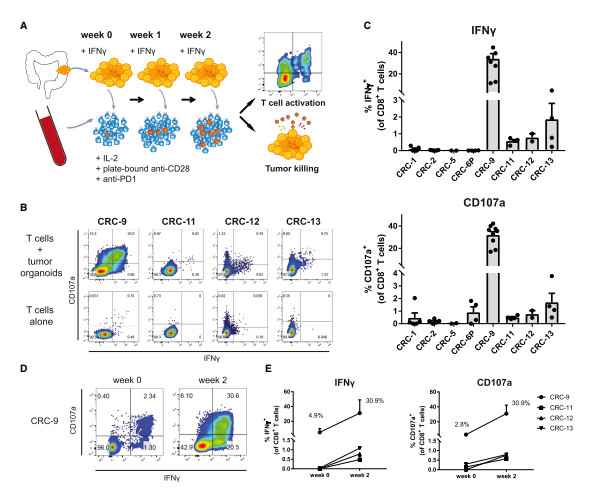
然后研究者将这些自体T细胞 - 肿瘤类器官共培养物用于评估T细胞介导的肿瘤破坏。通过流式细胞计数来量化活肿瘤细胞的数量,作者表明,与自体T细胞共培养导致细胞凋亡增加和肿瘤类器官瘤体缩小,但该作用不见于用自身健康组织培养的类器官。

重要提示:能够从少量活检组织中建立肿瘤类器官并刺激外周血(而不是需要分离肿瘤浸润淋巴细胞)肿瘤特异性CD8 + T细胞增殖, 提供了一种微创方法来研究患者特异性免疫反应和对各种疗法的敏感性。该技术还可以用于适应性T细胞治疗的个体化T细胞的获得。
|