|
|
作者:CardiothoracicSurgery

摘要
这是日本食管学会于2022年出版的英文版第12版《日本食管癌分期》的前半部分。
注:内容篇幅较长,翻译不知之处还请各位看官指正!
前言
《日本食道癌分类》第12版是在2015年第11版出版7年后出版的。考虑到术前治疗的重要性日益增加,我们对术前诊断的描述进行了补充和修改,特别是被认为对治疗政策有重大影响的T4和淋巴结转移的诊断,并修改反应评估标准,并确保与日本癌症分期手册保持一致,特别是对于食道胃交界处的癌症。上一次修订的目的是尽可能与国际癌症控制联盟(UICC)的TNM分期保持一致。然而,与N分期的一致性被忽略了,因为我们的N分期是基于相对于主要肿瘤的位置,并且在锁骨上淋巴结转移的观点上完全不同。这一新版本采用了基于转移数目的分类,与TNM分期一致。此外,通过检查清扫疗效指数和复发频率,制定了更符合临床实际的区域淋巴结。根据这些淋巴转移分期的变化,在一个术前治疗已成为标准的时代,我们利用国家食道癌综合登记处的预后信息开发了一种新的分期系统。
确定了食管胃交界癌的诊断标准,并在以前的版本中增加了一本七页的手册。在这次修订中,食道胃交界癌的定义和描述是由日本胃癌协会共同制定的。此外,还建立了食管胃交界癌的区域淋巴结,并增加了对分期的描述。委员会成员之间进行了多次讨论,促成了这次修订。虽然仍有一些问题需要讨论,但我们感谢各位委员所作的努力。
第12版总则
1.剔除“Ae”作为食道的一个亚位,将“Jz”新定义为食管胃交界区。“Jz”等于Nishi分期中的食管胃交界区。
2.我们将cT3细分为可切除(cT3r)或边缘可切除(CT3br),因为在影像上很难确定邻近器官受累。在cT3r、cT3br和cT4的诊断中增加了参考CT图像和辅助发现。
3.对于 cN 的诊断,参考 CT 诊断中淋巴结转移大小的诊断准确性,提供了推荐的临界值。使用 PET 进行诊断也可作为参考。
4.为了与TNM分期相一致,采用了基于区域转移性淋巴结数目对淋巴结转移程度进行分期。在此基础上,我们放弃了胸段食道癌与肿瘤部位相关的淋巴结分组,重新建立了胸段食道癌常见的区域淋巴结。锁骨上淋巴结被归类为远处而非区域性。因为在某些情况下可以清扫,所以它被定义为M1a,以区别于其他远处转移(M1b)。虽然106pre、106tbR和112aoP经常在转移阳性病例中予以清扫,但由于缺乏关于清扫疗效指数的数据,在本版中它们被定义为远处转移癌M1b。
5.在每种类型的食道切除术中,根据淋巴结清扫的模式和范围来确定淋巴清扫的程度(D)。胸段食道癌:D1:清扫<D2;D2:两野淋巴结清扫;D3:D2+颈部淋巴清扫。我们将106tbl、111、8a和11p包含在标准D2解剖范围内,但可以省略。
6.随着局部晚期食管癌术前标准治疗的流行,根据最新数据将分期分为临床分期和病理分期。
7.我们与日本胃癌协会共同建立了食道胃交界癌的定义和描述,组织开展全国胃癌、食道癌登记管理工作,为今后进一步开展研究工作提供方便。
8.尽管在RECIST的治疗效果判定标准中,原发食道癌是非-靶病灶,它对预后的影响是显著。因此,我们开发了一个指标来判断CT对原发病灶的疗效。同时,更新了用内镜确定原发肿瘤治疗效果的标准。此外建立了内窥镜判断CR(完全缓解)后局部复发的诊断标准。
9.根据内镜诊断和治疗的进展,日本食道协会浅表性食管癌深度扩大内窥镜诊断标准委员会制定的分类内容(2012年9月)在参考术语中描述。
10.鳞状上皮内瘤变重新评估和修订。
11.先前存在的手术结果(手术大体结果、术中成像结果和切除标本大体结果)和内窥镜治疗结果[e](术中和切除标本大体结果)被纳入最终分析,并从列表中删除。
缩写
A Anterior 前部的
AD Adventitia 动脉外膜
AI Invasion to the adjacent organs 侵袭邻近器官
APC Argon plasma coagulation 氩等离子凝固
BA Brownish area 褐色区域
BLI Blue laser imaging 蓝色激光成像
Br Borderline resectable 边缘可切除
c Clinical findings 临床表现
Ce Cervical esophagus 颈段食道
CR Complete response 完全缓解
CRT Chemoradiotherapy 放化疗
CT Chemotherapy 化疗
CTV Clinical target volume 临床靶区体积
D Extent of lymph node dissection 淋巴清扫范围
DM Distal margin 远端边缘
DMM Deep muscularis mucosae 深部粘膜肌层
E Esophagus 食管
EGJ Esophagogastric junction 食道胃交界处
EI Esophageal invasion 食道浸润
EMR Endoscopic mucosal resection 内窥镜下粘膜切除术
EP Epithelium 上皮
ER Endoscopic resection 内窥镜下切除术
ESD Endoscopic submucosal dissection 内窥镜下黏膜下剥离术
f Final findings 最终结果/诊断
G Stomach 胃
GI Gastric invasion 胃浸润
GIST Gastrointestinal stromal tumor 胃肠道间质瘤
HH Hiatus hernia 裂孔疝
HM Horizontal margin 水平边缘
HT Hyperthermia 过高热
IM Intramural metastasis 壁内转移
INF Infiltrative growth pattern 浸润生长模式
IO Immuno-oncology drug 免疫肿瘤学药物
Jz Zone of esophagogastric junction 食管胃交界区
Laser Laser therapy 激光疗法
LPM Lamina propria mucosae 粘膜固有层
LR Local recurrence 局部复发
LSBE Long-segment Barrett’s esophagus 长段巴雷特食道
Lt Lower thoracic esophagus 下胸段食道
Ly Lymphatic invasion 淋巴管浸润
Ly/V Lymphatic invasion or venous invasion 淋巴管侵犯或静脉侵犯
M Distant organ metastasis 远处器官转移
MCT Microwave coagulation therapy 微波凝固疗法
MM Muscularis mucosae 粘膜肌层
MP Muscularis propria 固有肌层
Mt Middle thoracic esophagus 胸中段食道
N Grading of lymph node metastasis 淋巴结转移的分级
NBI Narrow band imaging 窄带成像
p Pathological findings 病理发现/诊断
P Posterior 后部
PD Progressive disease 进展性疾病
PDT Photodynamic therapy 光动力疗法
Ph Pharynx 咽
PM Proximal margin 近端边缘
PR Partial response 部分反应
R Residual tumor 残留肿瘤
RECIST Response evaluation criteria in solid tumors 实体瘤的疗效评价标准
RM Radial margin 放射状边缘
RR Remarkable response 反应显著
RT Radiotherapy 放疗
SCE Specialized columnar epithelium 特化柱状上皮
SCJ Squamocolumnar junction 鳞状柱交界处
SD Stable disease 稳定期疾病
SIN Squamous intraepithelial neoplasia 鳞状上皮内瘤变
SM Submucosal layer 粘膜下层
SMM Superficial muscularis mucosae 浅部粘膜肌层
SSBE Short‑segment Barrett’s esophagus 短段巴雷特食道
T Depth of tumor invasion 肿瘤侵袭深度
Te Thoracic esophagus 胸段食道
Tis Carcinoma in situ 原位癌
Ut Upper thoracic esophagus 上胸段食道
V Venous invasion 静脉浸润
VM Vertical margin 垂直边缘
X Cannot be assessed 无法评估
淋巴结相关的学术语
R Right 右
L Left 左
Sm Submandibular 下颌下的
spf Superficial 表浅的
ac Accessory 附件
tr Tracheal 气管的
up Upper 上部的
mid Middle 中部的
rec Recurrent nerve 喉返神经
tb Tracheobronchial 气管支气管的
pre Pretracheal 气管前的
ao Paraaortic 主动脉旁的
pul Pulmonary ligament 肺韧带
总则
1.目的、对象和描述方法
1.1目的
食道癌临床和病理研究指南最初由日本食道病学会于1969年出版。自那以后,该协会于2003年更名为日本食道学会,并在日语中发布了“日本食道癌分类”,对治疗结果进行了修改,以保持最新情况并提供标准的命名法。该协会正在出版一本英文手册,题为《日本食道癌分期》,以促进指南和分期在国际上的使用。
1.2对象
日本分期中的食道癌是指起源于食道的癌症,不包括转移到食道的癌症。所有的食道原发恶性肿瘤都应根据日本的分期进行描述。
1.3描述方法
1.3.1描述和缩略语的原则
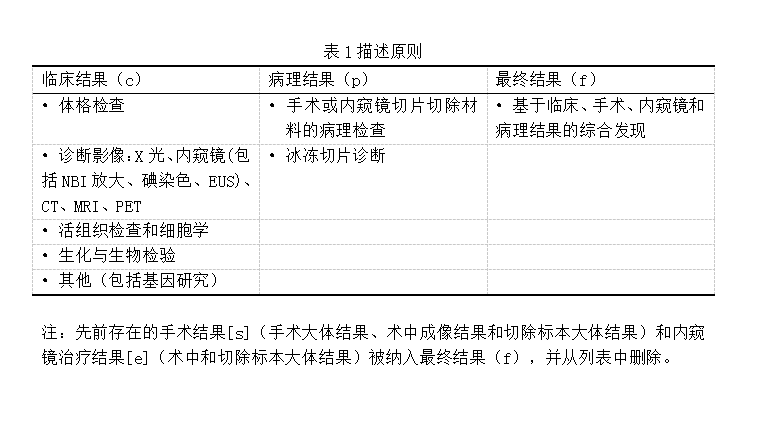
结果用大写字母T(肿瘤侵袭深度)、N(淋巴转移)和M(远处器官转移)记录。每个大写字母后面都有阿拉伯数字来表示每个结果的程度。“X”用于未知情况。在每个大写字母之前,分别使用小写的“c”、“p”和“f”来标识三类发现,即临床、病理和最终发现。可以省略最终结果的“f”(表1、2)。描述日本食道癌分期的清单如表3和表4所示。
临床描述顺序为:肿瘤部位(包括距切牙的距离)、侵犯范围、肿瘤长度、肿瘤大体类型、组织学类型(确诊时)、肿瘤侵犯深度、淋巴结转移、远处器官转移、分期,如:Mt(31~36 cm)、周长及前壁1/2、5 cm、2型、中分化鳞癌、cT3、cN2、cM0、cStage IIIB。
病理描述顺序如下:肿瘤部位、肿瘤长度、肿瘤大体类型、组织学类型、肿瘤侵袭深度、浸润性生长方式、淋巴管侵犯、静脉侵犯、壁内转移、切缘(近端、远端和放射状切缘)受累、多发性原发癌、化疗和/或放疗的组织学反应、淋巴结转移、远处器官转移和分期,例如:Mt,5 cm;2型,中分化鳞状细胞癌;pT3, INFa, Ly1a, V1a,pIM0, pPM0, pDM0, pRM0,多原发癌(现有2个病灶)、CRT-Grade 2、PN1(2/30)、sM0、fStageIIIA。
其他需要填写的项目:1.其他器官转移与癌侵袭 2.非癌并存肿瘤:平滑肌瘤及其他 3.其他:Barrett‘s食道、贲门失弛缓症及其他基础病变



2.原发肿瘤的描述
2.1原发肿瘤的数量、大小和环周位置
应描述肿瘤的最大长度(mm)、正交方向的最大宽度(mm)、环周范围的中心以及肿瘤在整个环周范围中所占的比例。此外,应记录所使用的诊断方法,如X线摄影、内窥镜检查和电子超声检查。
2.2肿瘤位置
2.2.1食道的解剖学定义
食管在解剖学上的定义是从食管口延伸到食管胃交界处。食管开口位于环状软骨下缘。食管胃交界处(EGJ)的鉴定将在第二部分中进行描述(请参阅第二部分中8.1)
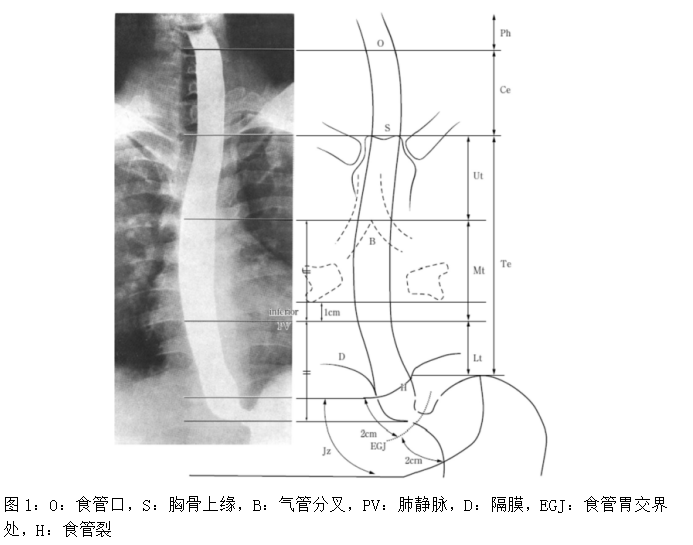
2.2.2食管的解剖亚部位(图 1)
食道位于下咽和胃之间,在解剖上可分为颈段食道(Ce)、胸段食道(Te)和食管胃交界区(JZ)。颈段食道(Ce):从食管口到胸骨切迹。
胸段食道(Te):从胸骨切迹至食管胃交界处头侧2厘米。
上胸段食道(Ut):从胸骨切迹到气管分叉
中胸段食道(Mt):气管分叉与食管胃交界处之间两个相等部分的近半段
下胸段食道(Lt):从Mt的下缘到食管胃交界处头侧2厘米
食管胃交界区(Jz):定义为食管胃交界处上方2厘米、食管胃交界处下方2厘米的区域。
注1:在无食道造影术的情况下,Mt和Lt的边界应该在CT 显示的下肺静脉下缘远端 1 厘米处。
注2:当JZ因食道裂孔疝进入胸腔时,首先应根据食管胃连接情况确定JZ的范围。然后,将剩余范围定义为Lt。
2.2.3肿瘤部位描述的原则
当由于除内窥镜检查以外的其他检查尚未进行导致肿瘤位置不确定时,仅描述距切牙的距离。
当肿瘤连续扩展到食道的一个以上部分时,肿瘤的主要位置是肿瘤侵袭最深的部位,应该首先描述这个部位。当肿瘤侵犯最深部位难以确定时,可记录肿瘤中心点部位为主要肿瘤部位。
在多原发灶的情况下,其位置按肿瘤侵袭深度的顺序进行描述。首先描述最深的病变。当很难确定深度的顺序时,描述的顺序取决于病变所占区域的大小。首先描述最大的病变,例如MtLt, LtJzG, CePh.
食管胃交界癌(请参阅第II部分8.4)
1.病变的位置应根据肿瘤中心的不同描述如下:E、EG、E=G、GE或G
2.肿瘤中心以距食管胃交界处的距离(-2 cm、+1 cm等)记录。-表示肿瘤中心位于食道,+表示肿瘤中心位于胃。
3.近端和远端侵犯的长度记录为距EGJ的距离(厘米)。
4.记录Barrett‘s食道、裂孔疝及其他并存病变。
2.3大体(肉眼)肿瘤类型
2.3.1肉眼肿瘤分型原则
肿瘤类型的分类是基于肉眼所见。放射学发现和内窥镜发现也根据肉眼发现来定义。
局限于粘膜或粘膜下层的肿瘤被归类为浅表型,而侵犯固有肌层或以上的肿瘤被归类为进展型。浅表类型以”0”为前缀,分为0-I、0-II或0-III。进展型分为四类:1、2、3或4。当肿瘤不能归入这5(0-4)类中的任何一类或由它们的组合组成时,它被归类为5
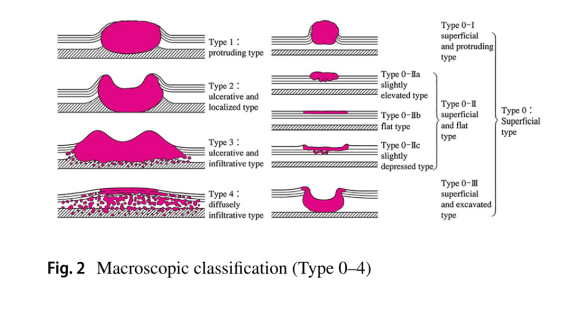
2.3.2肉眼肿瘤类型(图2、3、4、5、6、7)
Type 0:浅表型
Type 1:隆起型
Type 2:溃烂局限型
Type 3:溃烂浸润型
Type 4:弥漫性浸润型
Type 5:无法分类
Type 5a:未经治疗不可分类
Type 5b:治疗后不可分类(注1、2)
注1:描述治疗前的肉眼肿瘤类型。
注2:如果是以前的治疗,如果肿瘤仍然可以分类为0-4型,请描述它,否则描述为5b型。在任何一种情况下,所有表示先前治疗的前缀,如CT-、RT-、EMR-,都应标明。


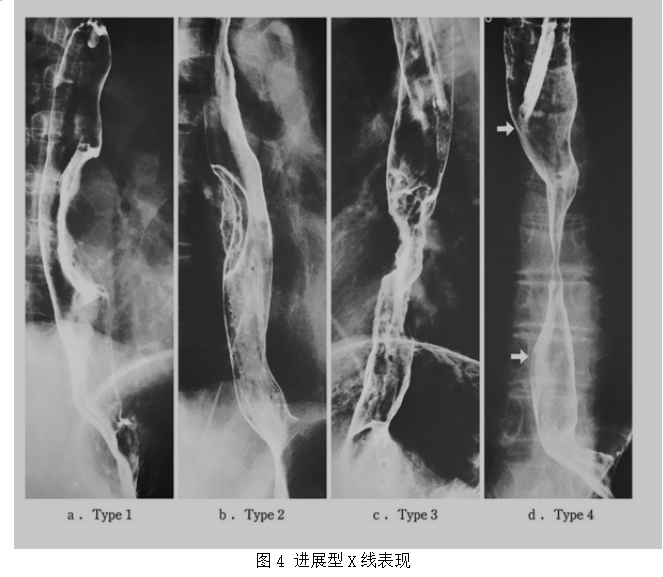
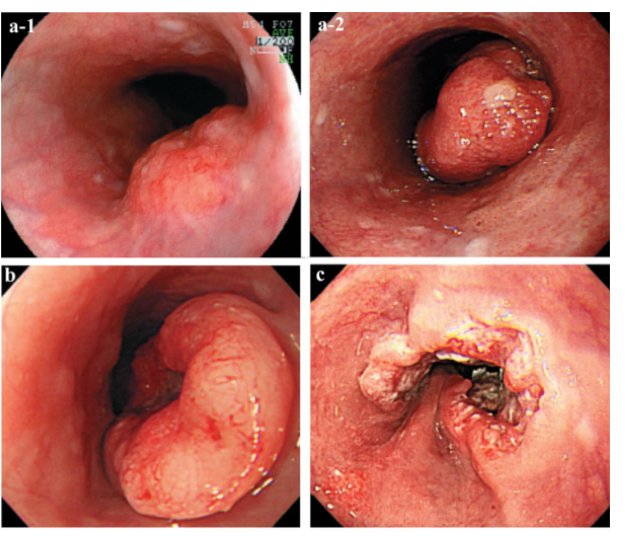
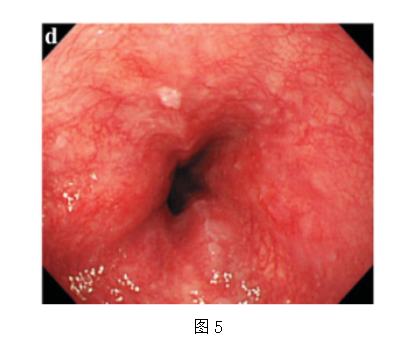
a-1 Type 1隆起型(pT2):底部较宽的高大病变。
a-2 Type 1 隆起型(pT2):底部狭窄的高大病变。
b Type 2, 溃烂局限型(pT3)。一种深溃烂的病变,周围有一条分明的脊线。
c Type 3,溃烂浸润型(pT3)。一种深溃烂的病变,周围有界限不清的隆起。
d Type 4,弥漫浸润型(pT3)。可观察到边界不清的食管壁增厚和硬化并伴有管腔狭窄。没有明显的溃疡形成。
2.3.3浅表类型(Type 0)的细分(图6和图7)
Type 0-I:表浅而突出
Type 0-Ip:有蒂的
Type 0-Is:无柄的(宽基底)
Type 0-II:表浅而平坦
Type 0-IIa:略微升高
Type 0-IIb:平坦
Type 0-IIc:略微凹陷
Type 0-III:表浅而凹陷
其他标注:
注1:混合型:当多种肉眼肿瘤类型混合在一个病灶中时,称为混合型。首先描述的是较宽大的肿瘤,其次是较小的肿瘤。双引号(“”)被放置在肿瘤侵袭最深的肉眼肿瘤类型周围。主要的肉眼肿瘤类型是深部肿瘤。但晚期类型被混合时,将首先描述最晚期的类型,不需要使用双引号。例如,0-IIc+“0-Is”,3+0-IIc。
注2:浅表性播散型:浅表型0-IIc型,肿瘤最大长度纵向延伸≥5 cm。这也可以在肉眼的肿瘤类型中描述。
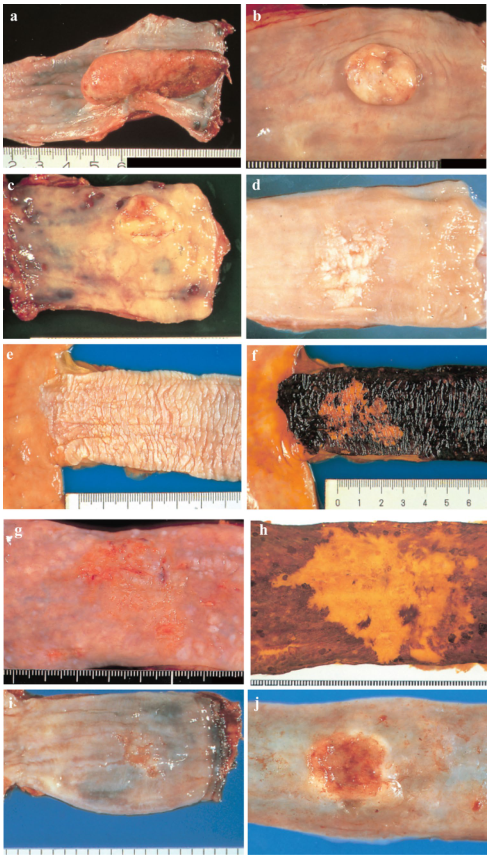
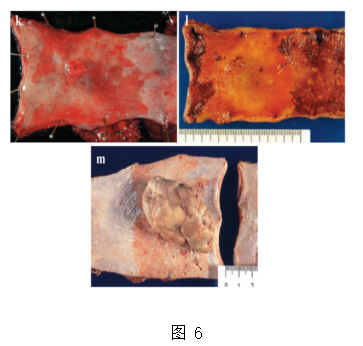
a Type 0-Ip(表浅的,突出型,带蒂型)肿瘤边界清楚,基底部狭窄。
b Type 0-Ip(表浅的、突出型、带蒂型)边界清楚、突出的肿瘤表面不规则结节。
c Type 0-Is(表面突出型,无柄)边界不清的肿瘤表面大部分被正常的附属膜覆盖。
d Type 0-IIa(略微升高)肿瘤一般为白色,仅从粘膜轻微隆起。
e Type 0-IIb(平坦)只观察到微小的不规则性,没有肉眼的异常特征。
f Type 0-IIb(平坦)被碘染色的标本e。浅层肿瘤未被碘染色
g Type0-IIc(略微凹陷)浅表凹陷性病变边缘不清,表面细小颗粒状
h Type 0-IIc(被碘染色的标本g)浅层肿瘤未被碘染色。
i Type 0-IIc(略微凹陷)浅表凹陷性病变边缘不规则。
j Type 0-III(表浅而凹陷)边缘轻微抬高的深度凹陷性病变提示侵袭性超出粘膜
k Type 0-IIc +“0-IIa”(浅表性播散型)广泛分布的轻微凹陷的红色病变(0-IIc)在其中心有一个轻微隆起的病变(0-IIa),提示侵犯到粘膜下层。病变长度超过5厘米,定义为浅表性播散型。
I Type 0-IIc +“0-IIa”(浅表性播散型) (被碘染色的标本k)微红凹陷的皮损不能被碘溶液染色。
m Type0-IIc +“0-Ip”. 边界清楚、底部狭窄的隆起性肿瘤(0-Ip),周围有轻度凹陷性病变(0-IIc)。
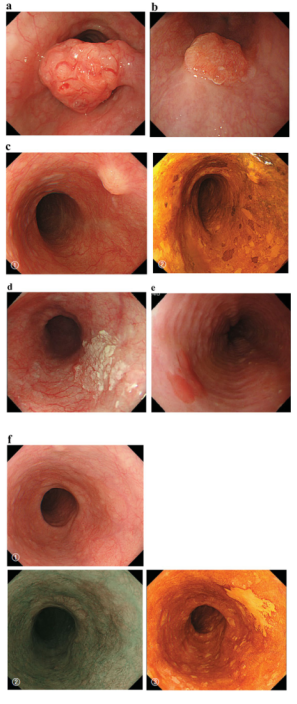
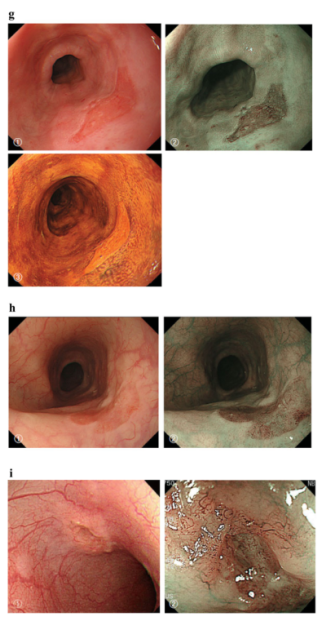
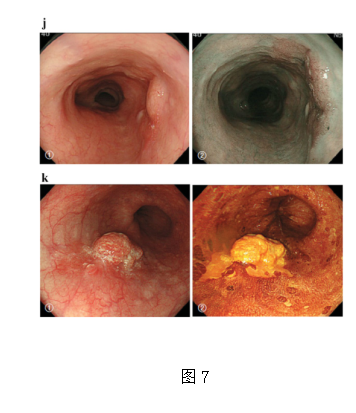
a Type 0-Ip,表浅、突起型和有蒂(cT1b-SM2-3)。边界清楚的突起和带蒂肿瘤显示不规则的结节状表面。
b Type 0-Is,浅表型,突起型和无柄(pT1b-SM2)。边界清楚的突起和无柄型肿瘤
c Type 0-Is,浅表型,突起型和无柄(pT1b-SM2)。1常规内窥镜检查:边界不清的隆起肿瘤被正常的食道黏膜覆盖,提示胸膜下有肿块。2碘染色:覆盖肿瘤的粘膜呈棕色,顶部未染色的区域提示裸露的肿瘤组织。
d Type 0-IIa,略微升高型 (pT1a-MM)斑块状、轻微隆起的白色肿瘤。白色区域的肿瘤侵袭仍在固有层内,而肿瘤远端边缘的微小突起侵犯粘膜肌层。
e Type 0-IIa,略微升高型(pT1a-EP),轻度隆起的肿瘤,边界清楚(0-IIa型病变高度小于1 mm)。
f Type 0-IIb,平坦(pT1a-EP),1常规内窥镜检查:常规观察不能发现病变。2窄带成像:可检出棕褐色区域。3碘染色:通过碘染色,完全扁平的病变被确定为边界清楚、未染色的区域。
g Type 0-IIc,略微凹陷型 (pT1a-LPM),1常规内窥镜检查:可见不规则形状的粘膜红变,并有轻微凹陷。2窄带成像:病灶也可见棕褐色区域。3碘染色:碘染色可见边界清楚、无染色的区域。
h Type 0-IIc,略微凹陷型 (pT1b-SM1),1常规内窥镜检查:可见粘膜变红,轻度凹陷,边缘隆起。2窄带成像:可见棕褐色区
域,提示多血管病变。
i Type0-III,表浅而凹陷型(cT1b-SM2-3),1常规内窥镜检查:可见明显凹陷的病变,周围有隆起区,提示溃疡已到达粘膜肌层。2窄带成像:边界清楚,周围隆起区呈棕褐色。
j混合型, 0-IIc+”0-Is” (pT1b-SM2).
1常规内窥镜检查:可见明显的隆起和较宽的底座。靠近远端边缘的轻微凹陷性病变也可观察到。2窄带成像:可见边界清楚的病变。
k混合型,0-Is+0-IIc (pT1b-SM2)
1常规内窥镜检查:可见明显隆起的病变,底部较宽,结节状不规则改变。怀疑病变附近的食道粘膜变红,边界不清。2碘染色:粘膜改变的边缘为界限清楚的未染色区域。
2.4肿瘤侵袭深度(T)(图8)
2.4.1肿瘤侵袭深度分类(T)
TX:无法评估肿瘤浸润深度
T0:没有原发肿瘤的证据
T1a:肿瘤侵犯粘膜 注1、2
T1a-EP:原位癌 (Tis)
T1a-LPM:肿瘤侵犯粘膜固有层(LPM)
T1a-MM:肿瘤侵犯粘膜肌层(MM)
T1b:肿瘤侵犯粘膜下层 (SM) 注1、3
T1b-SM1:肿瘤侵犯粘膜下层的浅三分之一
T1b-SM2:肿瘤侵犯粘膜下层的中间三分之一
T1b-SM3:肿瘤侵犯粘膜下层的深三分之一
T2:肿瘤侵犯固有肌层(MP)
T3:肿瘤侵犯外膜(AD) 注4
T4:肿瘤侵犯邻近结构(AI) 注5、6、7
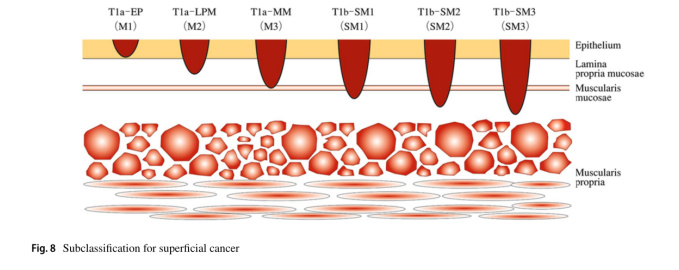
注1:浅表性食管癌:无论是否有淋巴结或远处器官转移,T1a和T1b均指定为浅表性癌,例如浅表性食管癌:T1NxMx。
注2:早期食管癌:无论有无淋巴结或远处器官转移,均可指定为T1a早期食管癌,例如早期食管癌:T1aNxMx。
注3:内镜切除的腺癌以外的癌标本中,肿瘤侵犯粘膜下层距粘膜肌层≤200μm的肿瘤被分类为T1b-SM1,而肿瘤延伸>200μm的肿瘤被分类为T1b-SM2。由于粘膜下层的真实整体厚度未知,因此未定义 SM3。在发生于食管或食管胃交界处的腺癌中,所有侵入粘膜下层且距离粘膜肌层>500μm的病变均被认为是T1b-SM2。对于 pT1b 癌,还测量距粘膜肌层下缘的侵袭距离。仅在内窥镜切除标本中描述侵入距离,例如 pT1b-SM2 (600 μm)。
注4:T3亚分类仅用于临床诊断。T3r:可切除:影像学上没有侵犯其他器官的证据。T3br:临界可切除:影像学上不能排除其他器官(气管、支气管或主动脉)的侵犯。描述怀疑被入侵的器官,例如,cT3br(气管)在本次临床T分类中,我们取消了cT4的亚分类。当怀疑肿瘤可切除而无需同时切除邻近器官时,应将其分类为cT3r。当肿瘤确实侵犯邻近器官时,即使邻近器官是胸膜、心包或膈肌,也记录为cT4。当可疑侵犯靶器官为气管、支气管或主动脉时,通常不同时切除,但未发现明确的cT4表现,则肿瘤归类为cT3br。
注5:T4亚分类仅用于病理诊断,不用于临床诊断。pT4a:胸膜、心包、膈肌、肺、胸导管、奇静脉和神经pT4b:主动脉(大动脉)、气管、支气管、肺静脉、肺动脉和椎体
注6:应记录侵犯器官,如心包、主动脉、腔静脉、气管、肺、膈肌、胸导管、喉返神经、奇静脉等,如cT4(肺)、cT4(主动脉)、pT4a (肺),pT4b(气管)。
注7:当转移淋巴结另外侵犯食管以外的周围器官时,应归类为T4,记录为“T4(转移淋巴结编号-受侵器官)”,例如cT4(No.112aoA-Aorta)。
注8:导管内受累定义为pT1a-EP。如果癌症侵犯食管腺管外,则深度由侵犯层数决定。
注9:若术前治疗后无存活且具有增殖能力的癌细胞,则分类为T0。在分期中,T0 与 T1a 同等使用。注10:食管腺癌的浸润深度分类对于颈部 (Ce) 和胸部 (Te) 食管腺癌,请遵循肿瘤浸润深度 (2.4.1.)”。根据《胃癌治疗》,食管胃结合部腺癌分类如下。
TX:肿瘤深度未知
T0:没有原发肿瘤的证据
T1:肿瘤局限于粘膜(M)或粘膜下层(SM)
T1a:肿瘤局限于粘膜(M)
T1a-SMM:肿瘤侵犯粘膜浅肌层(SMM)。
T1a-LPM:肿瘤侵犯粘膜固有层。
T1a-DMM:肿瘤侵犯深部粘膜肌层(DMM)。注11
T1b:肿瘤局限于粘膜下层(SM)
T2:肿瘤侵犯固有肌层(MP)
T3:肿瘤侵犯浆膜下层(SS)
T4:肿瘤侵犯邻近浆膜或暴露于浆膜之外,或肿瘤侵入邻近结构。
T4a:肿瘤侵犯邻近浆膜或穿透浆膜并暴露于腹膜腔(SE)
T4b:肿瘤侵犯邻近结构(AI/SI)
注11:如果存在新的粘膜肌层(粘膜浅肌层(SMM)),则粘膜深层肌层(DMM)被视为原始粘膜肌层。当肿瘤侵入 DMM 时,被称为 T1a-DMM。如果食管腺癌中未发现粘膜肌层重复,则应将其描述为 T1a-MM。
2.4.2放大内窥镜对浅表性食道癌深度的诊断标准
日本食道协会(JESA)使用放大内窥镜诊断浅表食道癌深度标准委员会(JESA)一直在研究在现有的两种内窥镜分类(井上分类和ARIMA分类)的基础上开发一种新的、更简单的分类。因此,我们发展了一种基于窄带光观察(NBI)和蓝激光成像(BLI)的新的分类方法,它是一种简单、客观的分类方法,对于区分肿瘤和非肿瘤以及评估肿瘤深度是有用的。
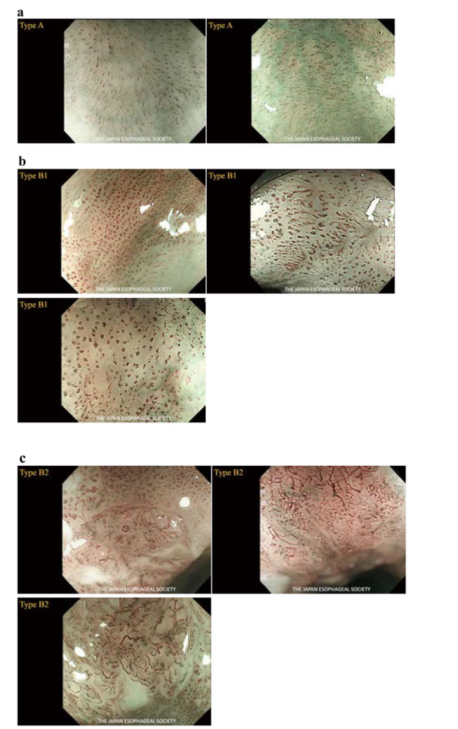
这种分类法是基于疑似鳞状细胞癌的具有地域性的病变。(注1)交界性病变的血管被归类为Type A。(注2)癌中可见的血管分为Type B,又分为B1、B2和B3型。T1a-EP和-LPM鳞状细胞癌的诊断结果为B1型,T1a-MM和T1b-SM1为B2型,T1b-SM2为B3型。
Type A:正常IPCL(上皮内乳头状毛细血管)(注3))或无严重不规则的异常微血管(图9a)
Type B:异常微血管,有严重的不规则或高度扩张的异常血管(图9B-g)
B1:呈环状排列的Type B血管(图9b)(注4)
B2:无环状结构的Type B血管(图9c)(注5)
B3:高度扩张的血管口径(图9d)(注6)
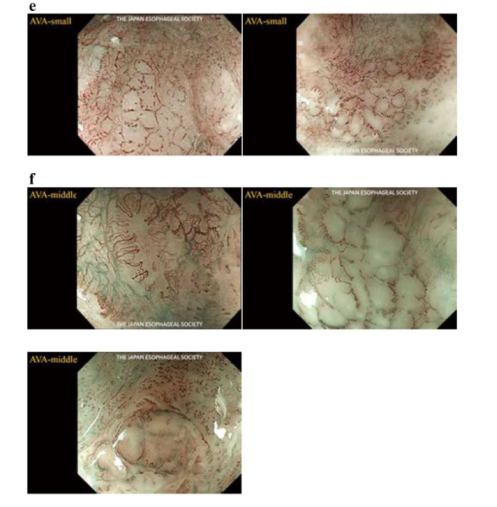
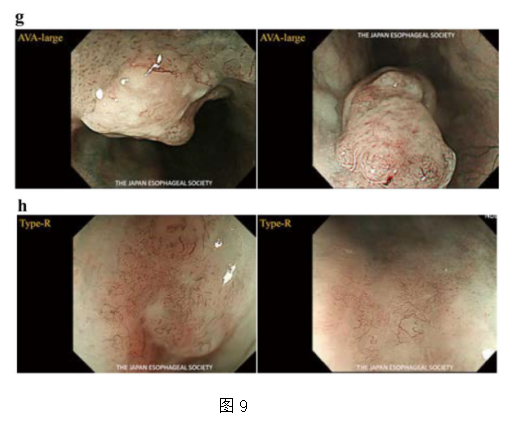
无血管区(AVA):AVA是无血管或有稀疏血管被Type B微血管(任何亚型)包围的特定区域。AVA分为三种类型:AVA-小型(直径<0.5 mm)(图9e)、AVA-中型(0.5 mm或0.5-3 mm之间)(图9f)和AVA-大型(≥3 mm)(图9g)。被B1血管包围的任何类型的AVA(小、中、大)均提示T1a-EP/LPM。AVA中型周围有B2或B3血管,提示为T1a-MM/T1b-SM1。被B2或B3血管包围的AVA大型提示T1b-SM2或更深。
网状微血管被定义为丛状微血管,并增加了“R”一词。这种血管模式常见于浸润性鳞癌或非鳞癌类型的恶性上皮性肿瘤(如基底细胞样鳞癌、腺鳞状癌和神经内分泌癌),其浸润性生长模式由单个细胞、小肿瘤巢或肿瘤细胞小梁排列(如INFc)组成。(图9h)
微血管之间的上皮呈棕色区域(BA:NBI或BLI显示的棕色上皮)被定义为血管间背景染色。
注1:边界可用正常或图像增强观察(染色、数字和光学数字方法)的病变
注2:主要为鳞状上皮内新增生性病变,但也可能包括炎症或癌。
注3:正常情况下,血管直径约为7-10μm。
注4:呈环状形态,如点状、螺旋状或绒毛状,血管直径约20-30μm。
注5:不形成环状的异常血管,如多层(ML)和不规则分支(IB)血管。
注6:不规则血管比B2血管大约3倍,血管直径大于约60微米。

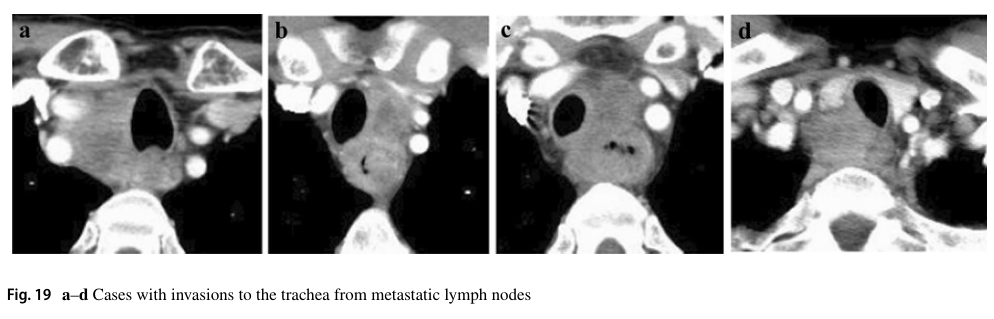
2.4.3 CT及其他影像技术诊断CT4侵犯邻近器官(图10、11、12、13、14、15、16、17、18、19、20、21)
这个分类系统取消了以前版本中作为临床诊断的T4的亚分类。然而,在实践中,目前尚不清楚肿瘤是cT3还是cT4,或者是可以切除的,还是不能切除的。在有明显邻近器官受累的
病例中,如食管瘘,cT4的诊断很容易,但邻近器官受累往往很难诊断。临床上的问题是,是否可以在不切除邻近器官(气管、支气管和主动脉)的情况下实现R0。因此,我们将cT3分为两类,cT3br(交界性可切除)和cT3r(可切除),前者不能排除邻近器官的侵犯,后者可排除邻近器官的侵犯。当肿瘤被认为侵犯邻近器官时,即使邻近器官是胸膜、心包或隔膜,它也被记录为cT4。当肿瘤可能侵犯邻近器官(如气管、支气管或主动脉),这些器官通常不能切除,但没有明确的cT4发现时,该肿瘤被归类为cT3br。
当原发肿瘤或淋巴结转移与呼吸道接触的边缘的层状结构不清楚时,以及当呼吸道受压、移位或管腔狭窄时,可诊断为气管和支气管侵犯。除了CT图像,评估支气管镜检查结果也很重要。
当原发灶或淋巴结转移灶与主动脉接触缘的层状结构不清,≥头尾长10mm可检出≥110°接触角(Picus角),或≥头尾长20mm可检出90~110°接触角(Picus角),即可诊断主动脉受侵。此外,如果肿瘤轮廓塌陷并接触或包围主动脉,则诊断为主动脉侵犯。
考虑到原发肿瘤的主壁位置(如后壁占优势或次全壁)和原发肿瘤的大体类型(隆起或溃疡),除增强CT外,还可使用上消化道内窥镜和食道造影来作出CT4诊断。如有必要,可使用MRI和EUS来辅助诊断主动脉和气管壁结构。
本章列举了cT3r、cT3br和cT4的典型CT图像以供参考。对于每一张CT图像,显示了专家之间诊断的符合率。
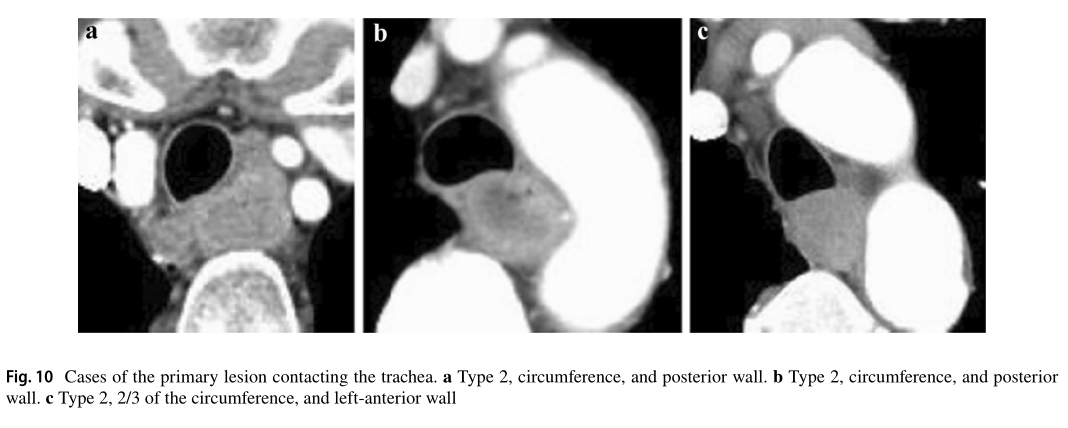
2.4.3.1典型CT图像:cT3r(图10、11、12)
我们展示了cT3r的典型CT图像,它没有侵犯到邻近的器官。我们提供日本食道癌分类委员会工作组的7位专家对肿瘤深度的符合率作为参考数据。原发灶在周围的偏侧性对气管侵犯的诊断有重要意义。尽管上段食道肿瘤经常压迫气管膜,但前段肿瘤和后段肿瘤侵犯气管的可能性不同。在这三幅图中,原发灶(位于食道上部)似乎与气管膜或气管软骨相接触。如图10a和图b所示,由于肿瘤位于后壁而且和气管之间有低密度层,因此不能确定气管侵犯,并且可以检测到肿瘤的强化轮廓。如图10c所示,我们确定没有气管侵犯,因为气管边界清楚,尽管存在左前部肿瘤,也没有观察到压迫、脱位或狭窄。
cT3的诊断符合率:10a,85.7%,10b,100%,10c,85.7%。
原发灶在周缘的偏侧性对诊断左主支气管瘤侵犯也有重要意义。在这三张图中,原发病变(位于食道中段)与左侧主支气管膜接触,似乎轻微压迫了它们。然而,三名患者都被诊断为无主支气管侵犯,因为可以检测到左主支气管与肿瘤强化轮廓之间的低密度层,没有发现支气管狭窄或畸形,肿瘤位于后壁。
cT3的诊断符合率:11a,100%;11b,100%;11c,100%。
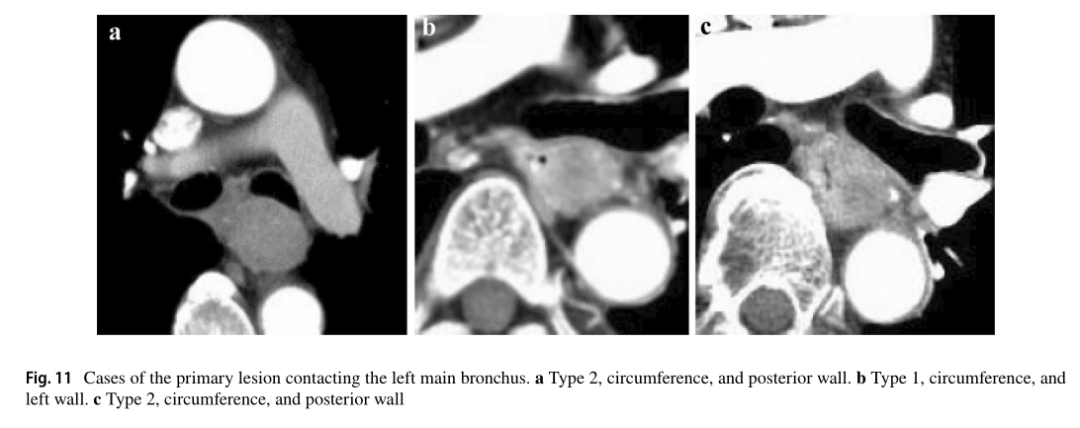
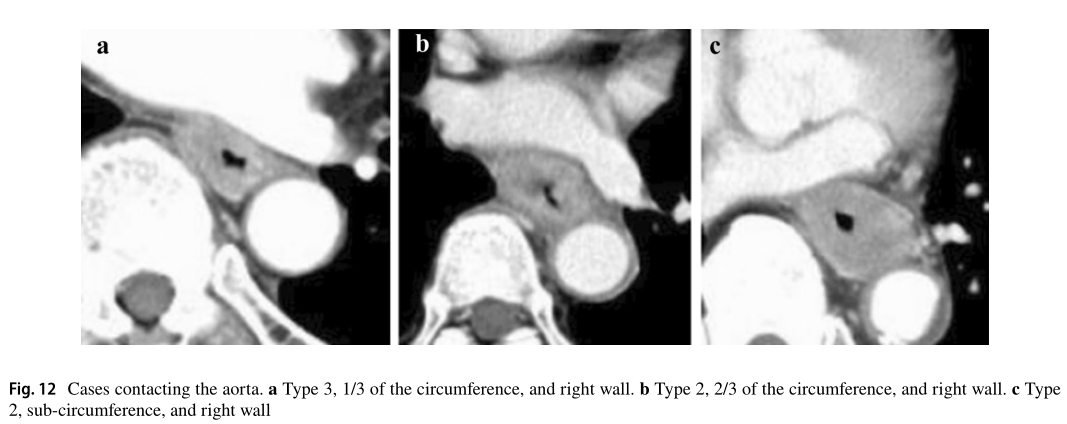
对于主动脉侵犯的诊断,原发灶在周缘的偏侧性也很重要。在这三张图中,原发灶(位于食道中段或下段)与降主动脉相接触。这三名患者都被诊断为没有主动脉侵犯,因为可以清楚地检测到原发病变和主动脉之间的脂肪层,并且他们的接触角(Picus角)<90°
cT3的诊断符合率:12a,100%;12b,71.4%;12c、100%
2.4.3.2典型CT图像:cT3br(图13、14、15、16)
我们提供了cT3br的典型CT图像,不排除侵犯邻近器官。
在这种情况下,≥110度的接触角(Picus角)可在头尾长度≥10 mm检测到,并可发现对主动脉的压迫。然而,肿瘤与主动脉接触的轮廓仍然存在,在主动脉和强化的肿瘤轮廓之间也可以检测到低密度层。总体而言,由于怀疑是cT4,此病例被诊断为cT3br
cT3诊断符合率:57.1%
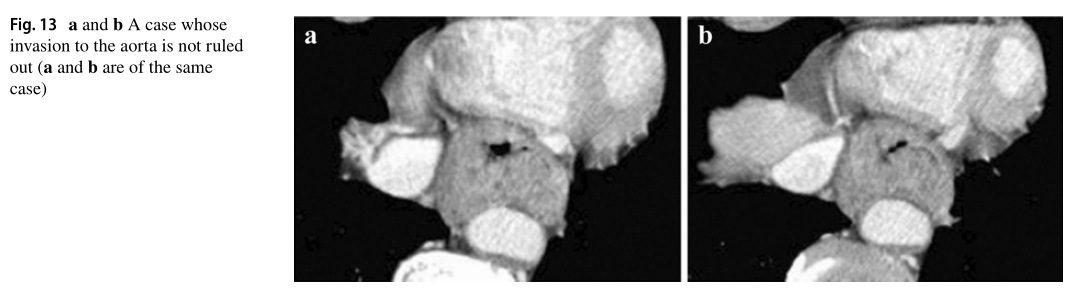
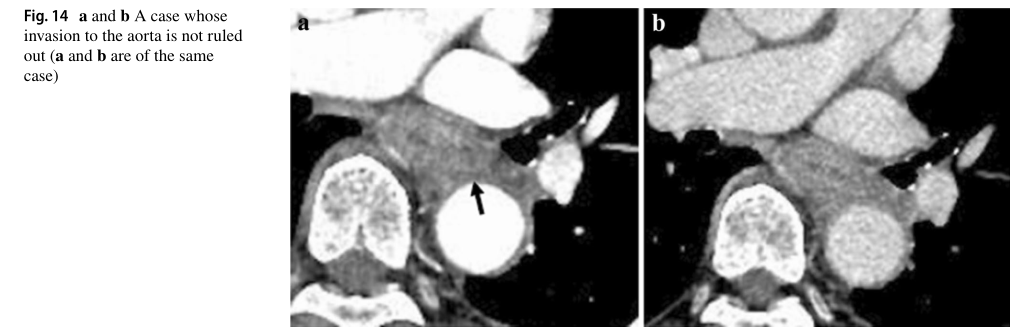
在本病例中,发现原发灶(位于食道上部)与大范围的气管膜和软骨及周围区域接触,但未发现气管受压、脱位、狭窄或变形。因此,结合cT4的怀疑,该病例被诊断为cT3br。
cT3诊断符合率:57.1%
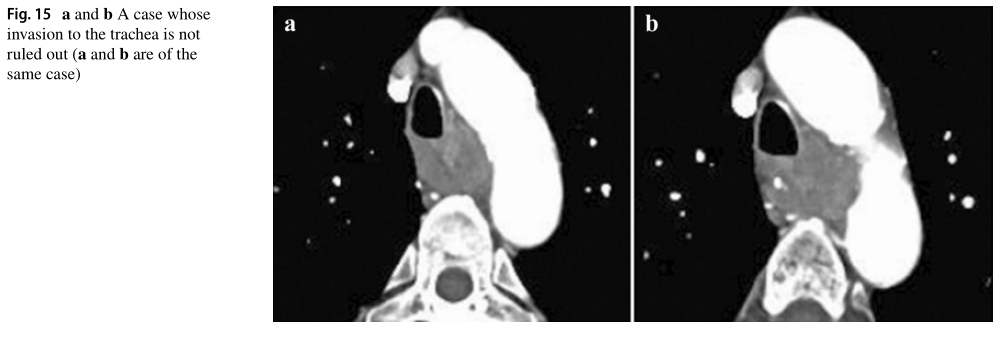
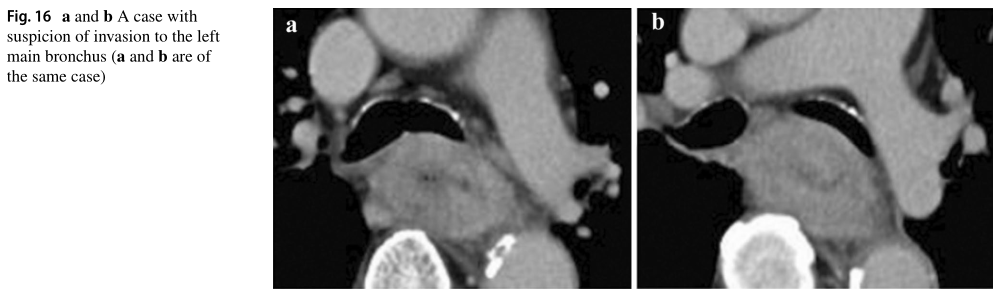
虽然食道上部的原发灶与左主支气管壁接触,但左主支气管处的压迫、脱位、狭窄和变形相对较轻和光滑。因此,在cT4的怀疑下,该病例最终被诊断为cT3br。
cT3诊断符合率:57.1%
2.4.3.3典型CT图像:cT4(图17、18、19、20、21)
我们展示了cT4的典型CT图像,认为它肯定侵犯了邻近的器官。
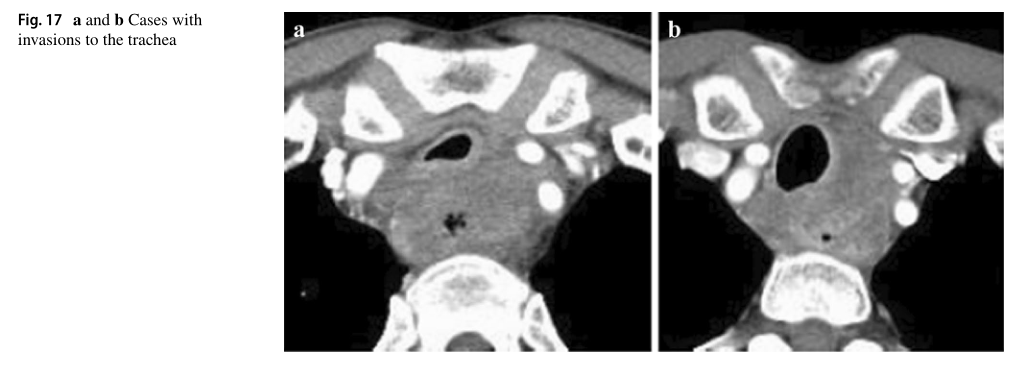
原发灶(位于食道上部)与气管膜和部分气管软骨接触。根据气管受压、脱位、狭窄和畸形的表现,这些患者被诊断为气管侵入。
cT4的诊断符合率:17a,85.7%;17b,85.7%
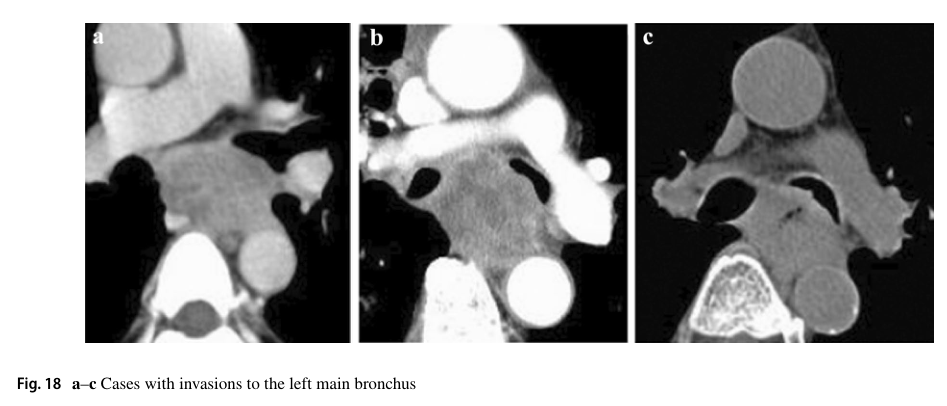
原发灶(位于食道中段)与左主支气管相接触,可见支气管膜受压、狭窄、变形。这些患者被诊断为左主支气管侵入。
cT4诊断符合率分别为18a,85.7%;18b,85.7%;18c,85.7%。
106recR或106recL转移结节广泛接触左右气管软骨和气管膜。观察到气管受压和脱位。这些病例被诊断为侵犯气管(cT4)。
cT4诊断符合率:19a,100%;19b,100%;19c,85.7%;19d,100%
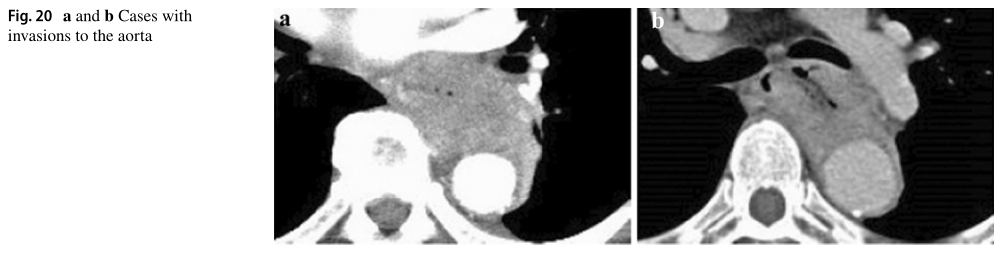
原发灶(位于食道下部)和主动脉之间的边界层模糊,接触角(Picus角)分别为160°(图16a)和110°(图16b)。这些病变似乎环绕在主动脉周围,这些发现在头颅和尾部图像中得到了证实(数据未显示)。这些患者被诊断为cT4。
cT4诊断符合率:20a,85.7%;20b,71.4%
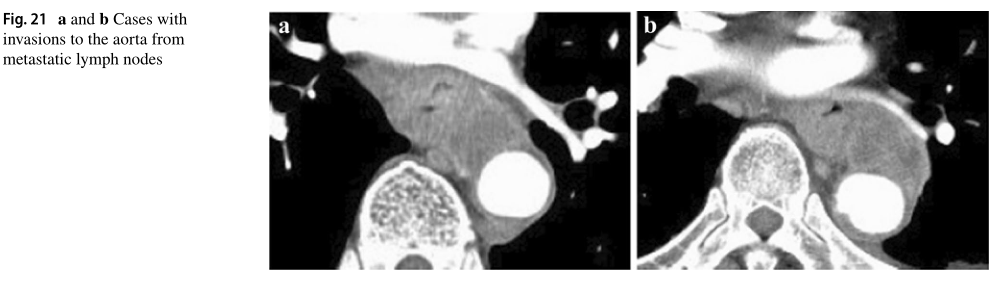
位于原发病灶(食管中段)和主动脉之间的108号转移淋巴结与主动脉相接触,失去了结节的边界。无法检测到边界层。接触角(Picus角)为100°(图21a)和120°(图21b),这些发现在头影和尾影(图未显示)中得到证实。这些病例被诊断为主动脉受侵。
cT4诊断符合率:21a,85.7%;21b,71.4%
2.5.浸润式增长模式(INF)
根据肿瘤边缘观察到的主要类型,肿瘤的浸润性生长类型可分为以下三种类型
INFa(膨胀型):肿瘤巢膨胀性生长,与周围组织边界清楚。
INFb(中间型):介于INFa和INFc之间的中间生长模式。
INFc(浸润型):肿瘤巢的浸润性生长,与周围组织边界不清。
2.6.淋巴或静脉侵犯
这些描述(Ly或V)仅用于病理结果,不用于临床结果。
注1:淋巴或静脉侵犯的不确定区分用Ly/V表示。
2.6.1淋巴侵袭(Ly)
LyX:淋巴侵袭无法评估。
Ly0:没有。
LY1:观察到淋巴侵犯。
Ly1a:轻微,累及一条或两条淋巴管。
Ly1b:中等。
Ly1c:严重。
注:在胸导管内发现的肿块被描述为淋巴侵犯阳性。
2.6.2静脉侵犯(V)
VX:静脉侵犯无法评估。
V0:无。
V1:观察到静脉受侵。
V1a:轻微,累及一至两条静脉。
V1b:中等。
V1c:严重
注:对于内窥镜下切除的标本,没有必要评估血管受累的程度;只需描述其是否存在。
2.7.手术发现的描述
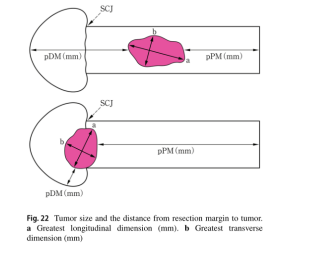
2.7.1肿瘤大小(图22)
最大纵向尺寸(mm)
最大横向(与肿瘤纵向轴成90°)尺寸(mm)
2.7.2手术切缘到肿瘤的距离(图22)
近端(口腔)缘(PM)(mm)
远端(肛门)缘(DM)(mm)
2.8 内窥镜检查结果的描述
2.8.1 肿瘤和切除标本的数量
病变数量
从每个病变中切除的标本数量
例如,1.整块切除;2.分割切除(分割切除是指病变被切除,但不是整块切除在这种情况下,应记录分割标本的数量。)
2.8.2 切除标本的大小和每个肿瘤病变的大小
尺寸描述为以毫米为单位的最大纵向尺寸乘以以毫米为单位的最大横向尺寸:a×b(mm)。
2.8.3 肿瘤类型
肿瘤类型被分类为Type 0-Ip, Type 0-Is,Type 0-IIa, Type 0-IIb, Type 0-IIc, Type 0-III,组合型等。
2.8.4切除切缘(注1、2)
对切除切缘的癌侵袭进行病理学评估,并对每个发现给予p-。病理和内窥镜检查结果综合判断为最终结果(f)。
2.8.4.1 水平边缘 (HM)(注3)
HMX:无法评估水平切缘是否有肿瘤残留。
HM0:所有水平切除切缘均证实非癌性鳞状上皮和固有层粘膜层。
HM1:肿瘤暴露在任何水平切除切缘上。
2.8.4.2垂直边缘(VM)
VMX:无法评估垂直边缘的残留肿瘤。
VM0:任何垂直边缘均无肿瘤暴露。
VM1:肿瘤暴露在任何垂直边缘。
注1:当在任何切除缘未发现肿瘤时,定义为完全切除(pR0);当在任何切除缘发现肿瘤时,定义为不完全切除(pR1)。
注2:切缘血管侵犯定义为切缘阳性(pHM1或pVM1)。
注3:分割切除病变时,应将重组标本的外缘视为水平边缘。
2.9 多发性原发癌
2.9.1 多发性原发食道癌
术语“多发性原发食道癌”是指存在两个或两个以上彼此分开的食道癌。它们应该与壁内转移灶分开描述。如果存在多原发癌,应描述每个病变的位置、大小、肉眼所见和肿瘤深度。在多个病变中,如果深度相同,则将原发灶定义为深度最深的病变或直径最大的病变。
注1:描述多原发癌的位置应按照肿瘤侵犯深度的顺序(从深到浅),在每个病变的位置缩写之间加上“/”,并在括号中记录病变的总数。例如,MtUt/Lt/Lt(3个病变)
注2:继发性病变在组织学上明显不同于主要病变,或具有相同的组织学特征,但有上皮内癌的证据,被认为是原发病变,并被视为多发性癌。
2.9.2 包括食道癌在内的多器官原发癌
包括食道癌在内的多器官原发癌是指食道癌以外的一种或多种原发恶性疾病在食道癌患者中的存在。
注1:如果多器官原发癌包括食管,括号内应注明食道以外的其他器官。
注2:应记录多发性是同步的还是异时性的,例如多器官原发癌:胃癌(同步)。
在一年内确诊的癌症被认为是同步癌症。在≥1年内确诊的癌症被认为是异时性癌症。如果同时和异时癌同时存在,则被认为是同步和异时癌。
2.10.壁内转移(IM)
肉眼上(清楚地)与原发灶分离的食道、咽或胃壁转移灶应记录为IM,并应描述此类病变的数目。
IMX:壁内转移不能评估
IM0:无壁内转移。
IM1:壁内转移。
注:壁内转移在胃壁应记录为“IM1-St”。这被归类为器官转移(M1)。
3.淋巴结的描述
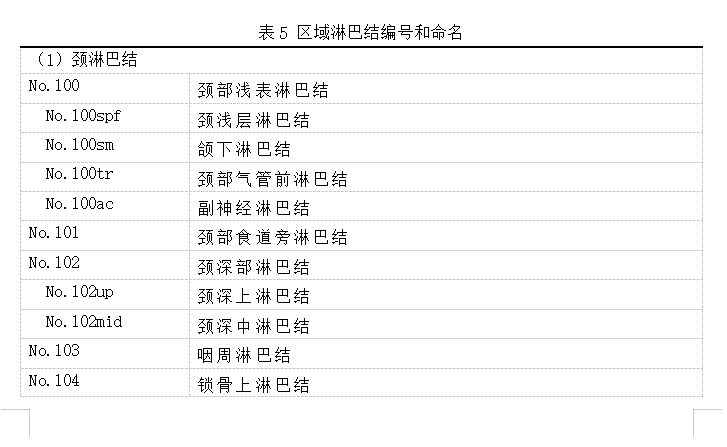
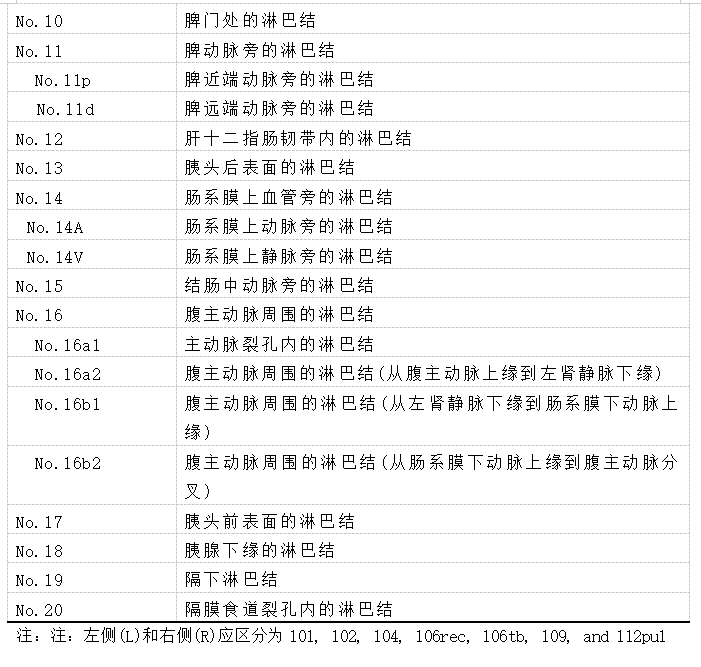
3.1. 食管癌淋巴结站点的名称、数目、范围和界限
淋巴结的名称和数量见表5和图23(见第II部分19)。
腹部淋巴结站的名称和数量是根据日本的胃癌分期来定义的.
注1:应用“No”记录淋巴结站的数目。加上一个数字,例如,No.106recR。
注2:CT和PET/CT诊断淋巴结转移的影像标准(见第II部分20)
•CT对淋巴结转移的诊断,增强CT层厚应为≤2.5 mm,
•基于限于cT2-T4患者的短径≥5 mm的淋巴结的分析,CT短径以6 mm为界值。然而,仅凭大小诊断淋巴结转移是有局限性的,因为大约1/3的转移淋巴结的短径<5 mm。
•虽然PET/CT在淋巴结转移的阳性预测价值方面优于CT,但由于机构间的差异以及受多种因素(患者的血糖水平、机器类型或协议)影响的可能性,SUV阳性的诊断标准尚未标准化。
•在PET-CT上,应注意纵隔淋巴结,特别是肺门区域的淋巴结,由于肺野炎症或结节病,可积聚FDG,导致假阳性结果。
注3:每个淋巴结站点记录转移和切除的结节数,例如 e.g., No.104R (0/10),No.104L (1/13), No.106recL (0/4)
注4:淋巴结外转移(肿瘤结节)是指在食道或胃以外的脂肪组织中无淋巴组织的癌巢,其数目和部位应记录为淋巴结外转移。
注5:应记录结外侵犯(直接或血管侵犯)。


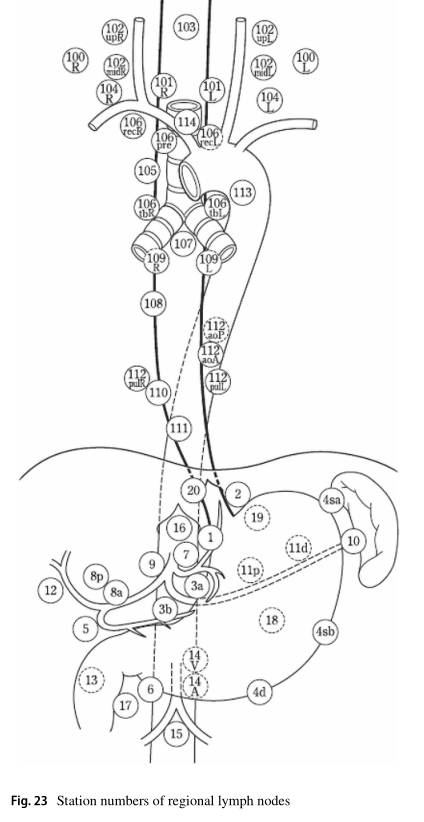
3.2区域淋巴结
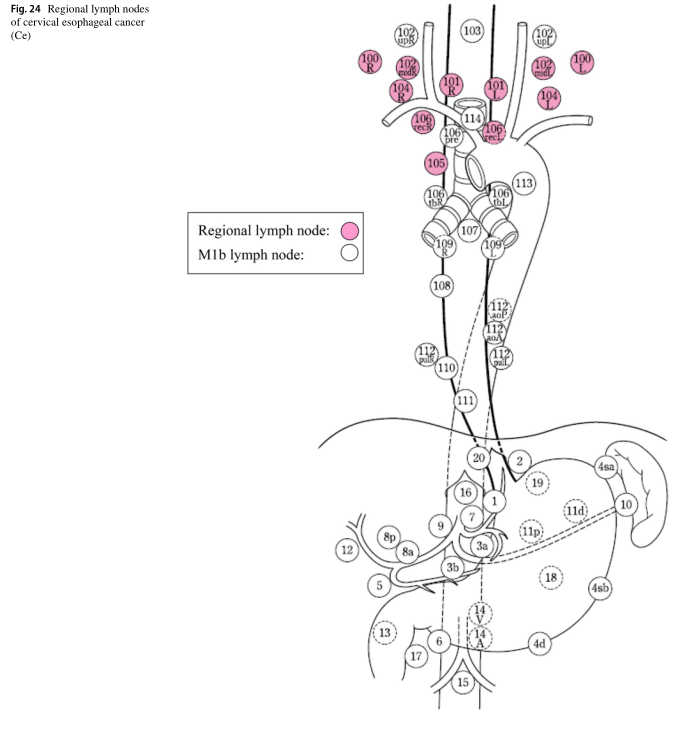
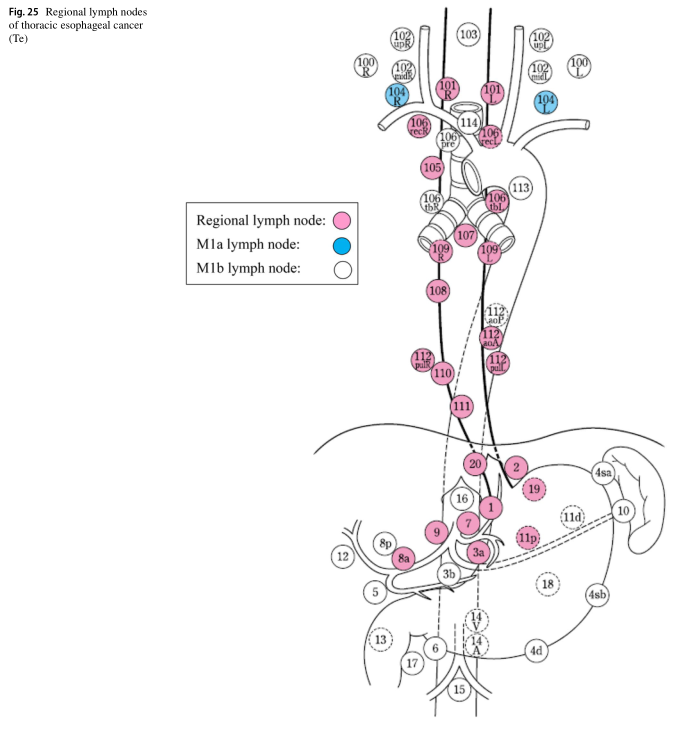
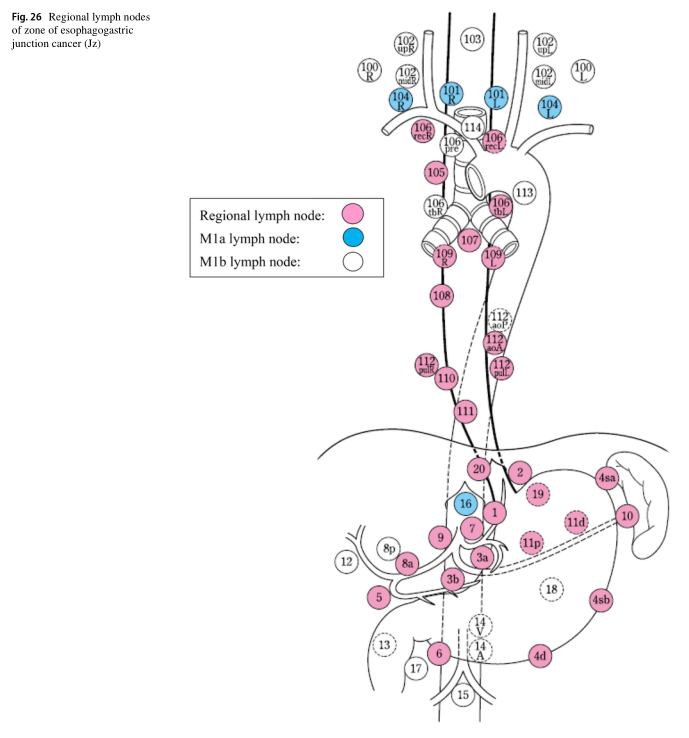
区域淋巴结是根据肿瘤的位置(Ce、Te和Jz)来定义的,如表6和图24、25、26所示。
注1:对于多发性食道癌或肿瘤连续侵犯食道的一个以上部位,应根据肿瘤侵犯最深的部位或主要肿瘤部位来确定区域淋巴结。
注2:在第11版《日本食道癌分类》之前,食道癌的淋巴结转移程度是按转移淋巴结的部位进行分类的。但在这一版本中,N分类改为根据国际癌症控制联盟(UICC)的TNM分类以转移淋巴结的数目为基础的系统。我们决定区域淋巴结的范围,以便患者可以从这些淋巴结的清扫中获得生存益处。淋巴结转移程度(N1-N3)是根据区域淋巴结转移的数目来确定的。
注3:区域淋巴结的概念
•胸段食道癌的锁骨上淋巴结(第104号)和食道胃交界处(JZ)癌的第101、104和16号淋巴结是区域外淋巴结;然而,我们将它们识别为M1a,以区别于其他M1b淋巴结,因为可以预期一些清扫的益处。
•上述M1a淋巴结(胸段食道癌第104号和食管胃交界部癌第101、104、16号)和其他区域外淋巴结(M1b)不包括在区域淋巴结转移数中。
•胸段食道癌的102、106pre、106tbR和112aoP淋巴结被归类为区域外淋巴结(M1b),因为预防性清扫的效果尚不清楚,尽管它们在转移病例中偶尔也会被清扫。

3.3.淋巴结转移分级(N)
NX:无法评估区域淋巴结转移
N0:无区域淋巴结转移
N1:转移至1至2个区域淋巴结
N2:转移至3至6个区域淋巴结
N3:转移至 7 个或更多区域淋巴结
对于淋巴结转移的病理诊断,颈、胸段食道癌以D2或以上淋巴结切除术为佳,食管胃交界部癌以D1+α或以上淋巴结切除术为佳(见5.3.3)。
4.远处器官和淋巴结转移(M)
MX:无法评估远处器官或区域外淋巴结转移
M0:既无远处器官转移,也无区域外淋巴结转移
M1a:区域外的淋巴结转移,但预计在清扫中具有一定的功效
M1b:既不是区域淋巴结也不是 M1a 的淋巴结转移,或远处器官转移
注:参考3.2区域淋巴结
远处器官转移应综合考虑手术肉眼所见、术中超声检查等术中影像检查、术中冰冻切片病理诊断及最终病理结果。应记录是否切除远处器官转移。
注1:远处转移的部位应记录如下:淋巴结(LYM)、皮肤(SKI)、肝脏(HEP)、肺(PUL)、骨髓(MAR)、骨(OSS)、腹膜(PER)、胸膜(PLE)、脑(BRA)、脑膜(MEN)、肾上腺(ADR)和其他(OTH)。
注2:胃壁内转移视为远处转移,记录为M1b(IM1-ST)。
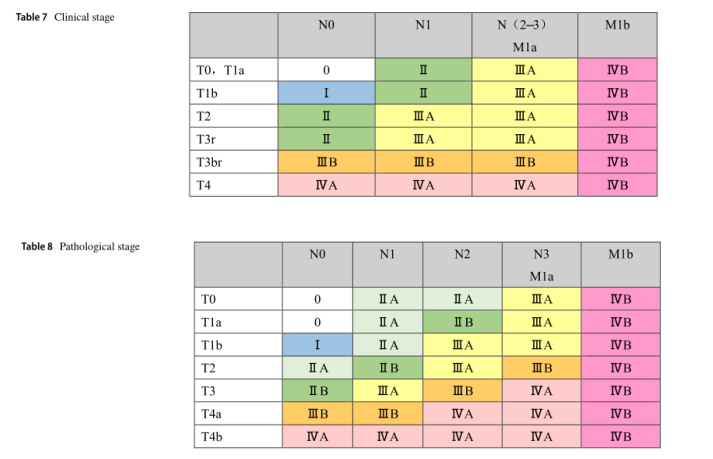
5.分期(表7、8、9、10)
记录T、N和M类别和分期,例如,T2N2M0,分期IIIA。
分期分为两类:基于影像诊断的临床阶段和基于切除标本的组织学检查的病理阶段。
5.1颈胸段食管癌和食管胃交界部鳞状细胞癌的分期
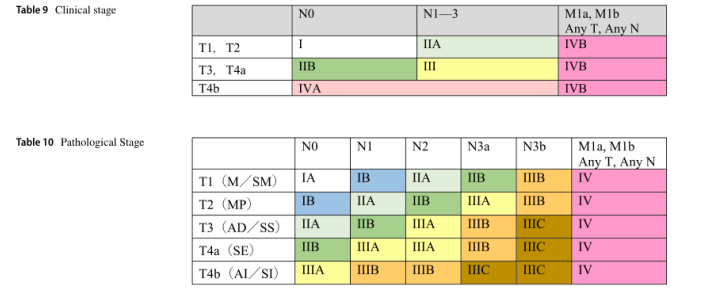
5.2食管胃交界部腺癌的分期
食管胃交界腺癌的分期应符合日本胃癌分类(第15版)(表9和10)。
5.3淋巴清扫程度和肿瘤残留
5.3.1淋巴结清扫
5.3.2淋巴清扫说明
两野清扫:清扫胸部和腹部淋巴结。必须清扫以下淋巴结:No. 101、105、106rec、106tbl、107、108、109、110、111、112aoA、112pul、1、2、3、7、8a、9、11p(清扫106tbl、111、8a和11p操作可以被省略)。
三野清扫: 颈部(注1)、胸部和腹部淋巴结被清扫。这相当于两野清扫加颈淋巴结清扫。
注1:颈部淋巴结清扫是指101、102、104号双侧淋巴结清扫,102号清扫可省略。101 号解剖可以从胸部进行。
注2:当未进行典型淋巴结清扫时,应描述淋巴结清扫范围,例如胸颈部淋巴结清扫(接受二期食管切除术但未进行腹部淋巴结清扫的患者)。
5.3.3淋巴清扫范围的定义(D)
根据食道癌的位置,淋巴清扫程度定义如下。
颈段食管癌(Ce)
DX:不能评估淋巴结清扫的程度
D1:低于D2的淋巴结清扫
D2:执行100、101、102 MID、104、105和106rec的淋巴结清扫(注1、2)
D3:不适用
注1:对于结节105、106recR和106recL,从颈部清扫是可以接受的。
注2:虽然淋巴结102是区域性淋巴结,但没有淋巴结102的淋巴结清扫术可视为D2
胸段食道癌(Te)
DX:无法评估淋巴结清扫的程度
D1:两野淋巴结不完全清扫
D2:两野淋巴结完全清扫
D3:三野淋巴结完全清扫
食管胃交界性癌(JZ)
D1:淋巴结清扫No. 1, 2, 3a, and 7(注1)
D1+:淋巴结清扫No. 1, 2, 3a, 7,8a, 9,and 11p(注2)
D2:淋巴结清扫No. 1, 2, 3a, 7, 8a, 9, 11p,19, 20, and 110(注3)
D3:淋巴结清扫No. 1, 2, 3a, 7, 8a, 9, 11p,19, 20, 105, 106recL, 106recR, 107, 108, 109L, 109R,110, 111, 112aoA, and 112pul(注4)
注1:在一项全国性前瞻性研究中,D1的范围等于结节有≥20%的转移率。
注2:在一项全国性前瞻性研究中,D1+的范围等于结节有≥10%转移率。
注3:食道侵犯长度2.1-4.0 cm者建议D2淋巴结清扫术。
注4:食道侵犯长度>4.0 cm者建议D3淋巴结清扫术。
注5:全胃切除时,在上述淋巴结范围内增加3b、4sa、4sb、4d、5和6。
注6:在本版中,D级是基于每个外科手术过程。根据一项全国性的前瞻性研究,淋巴结4sa和4sb被排除在应该切除的淋巴结之外,因为它们转移的频率很低
5.3.4内窥镜和手术切除后残留肿瘤(R)
RX:无法评估是否存在残留肿瘤(注5)
R0:无残留肿瘤
R1:显微下残留肿瘤(切缘或放射缘)(注2)
R2:大体残留肿瘤
注1:原发灶和转移灶均应评估残存肿瘤。
注2:根据冰冻切片或术中脱落细胞学检查,高度怀疑有微小残留肿瘤的病例按R1分类。
注3:当治疗多个病变时,每个病变的R分类是单独确定的。
注4:在分段切除的情况下,应尽可能在重建标本后对R分类进行评估。仅当重建是可能的并且在重建标本的切除边缘识别出非癌组织时,才能确认分段切除的pR0。
注5:RX
1.非癌性细胞因受挤压或烧毁的影响,不能在边缘确认。
2.重建标本不可能,因为是分段切除。
3.鳞状上皮基底层肿瘤扩展不连续,疑似残留肿瘤。
4.可能因导管内扩散而在垂直切缘残留肿瘤。
5.因其他原因无法确定的残留肿瘤。
6.经内窥镜及外科手术切除的样本的处理
6.1内窥镜切除标本的处理
标本取出后立即伸展固定在软木板或聚苯乙烯泡沫塑料上,并在足够量的10%中性福尔马林缓冲溶液中固定至少半天。
6.2手术切除标本(原发肿瘤)的处理
切除的食道应沿病变对侧的纵线切开。接下来,应该轻轻地纵向拉伸和固定,使标本的长度与体内的大小相似。无论是新鲜标本还是固定标本,都需要照相记录。标本切除后在软木板或聚苯乙烯泡沫上延伸,并固定在足够体积的10%中性缓冲福尔马林溶液中。建议固定时间<72h。
6.3切除标本的切片
6.3.1切片标本的准备
福尔马林固定的标本应用碘溶液处理,以确认未染色的区域,并准确识别和记录肉眼观察结果。这对浅表性癌的治疗很重要。对于内窥镜切除的标本,用自来水冲洗至少30分钟,对于手术切除的标本,至少冲洗1小时,将提供良好的染色条件。为了增加染色和未染色区域之间的对比度,应用较低浓度(0.1-0.5%)的碘溶液长时间处理样品。
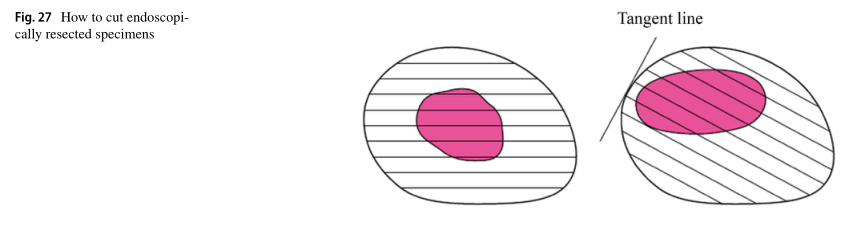
6.3.2内窥镜下切除标本的切片规则(图27)
切割线被定义为在最接近肿瘤的切缘处与切线成直角的交叉线,整个切除标本被切割成每片2-3 mm厚的切片。
6.3.3手术切除标本的切片规则(图28)
切除的标本应平行于食道的长轴切开。对于浅表性癌,应做好整体切片。晚期肿瘤侵袭最深处、平行或垂直于食道的有代表性的切片应被截取并用于显微镜检查。应将整个肿瘤切成切片进行肉眼观察,并选择合适的切片进行显微镜检查。根据肉眼所见,近侧缘的部分必须平行或垂直。应保存切面部位的图样或照片。

未完待续

长按二维码添加
关注我们 获取更多文献
点赞或分享 让我们共同成长

点击“阅读原文”看摘要原文 |
|