|
|
作者:中国医学论坛报今日肿瘤
2024年3月20日~23日,由欧洲肿瘤内科学会(ESMO)和国际肺癌研究学会(IASLC)举办的欧洲肺癌大会(ELCC)在捷克共和国布拉格成功举行。本届大会上,如何进一步优化晚期非小细胞肺癌(NSCLC)的诊疗依然是备受关注的热点话题。近年来,抗体偶联药物(ADC)在多个实体瘤中的探索取得耀眼成绩,靶向滋养层细胞表面抗原2(TROP2)的ADC在NSCLC领域的研究同样战绩不俗,不断刷新晚期患者的生存数据。
TROPION-Lung01作为首个探索ADC用于经治的有或无可靶向基因组改变(AGA)的局部晚期/转移性NSCLC患者取得阳性结果的Ⅲ期临床试验,其研究结果于2023年ESMO和欧洲肿瘤内科学会亚洲年会(ESMO ASIA)上重磅亮相。其中,Dato-DXd用于非鳞状NSCLC(NSQ-NSCLC)患者获益更佳,该亚组数据于本次ELCC再次更新,以高级别的循证医学证据为临床实践带来更多启示。值此学术盛会之际,本报特邀请辽宁省肿瘤医院马锐教授立足NSCLC未满足的治疗需求,解读TROPION-Lung01研究NSQ-NSCLC亚组更新数据,展望未来探索方向。
专家简历

马锐 教授
辽宁省肿瘤医院
胸内二科主任、硕士生导师
中国临床肿瘤学会理事会理事
中国老年学学会老年肿瘤专业委员肺癌分委会常务委员
中国医药教育协会肺部肿瘤、肿瘤免疫专委会常务委员
中国抗癌协会肺癌专业委员会委员
辽宁省抗癌协会理事会理事
辽宁省生命科学学会常务理事
辽宁省抗癌协会肿瘤转移专业委员会主任委员
辽宁省生命科学学会肺癌专业委员会主任委员
辽宁省抗癌协会肿瘤标志物专业委员会副主任委员
辽宁省药学会抗肿瘤药物专业委员会副主任委员
沈阳市医学会肺部肿瘤学分会副主任委员
沈阳市领军人才
获益受限
晚期经治NSCLC患者急需改善生存困局
基于精准治疗在肺癌领域的探索,靶向及免疫治疗为晚期NSCLC患者带来显著生存获益。然而,很多患者仍然不可避免面临获得性及继发性耐药问题[1-3]。《中国临床肿瘤学会(CSCO)NSCLC诊疗指南2023》推荐不伴AGA的晚期NSQ-NSCLC患者二线接受免疫单药或化疗(既往未使用该药),但中位无进展生存期(PFS)仅约3个月[4,5]。对伴有AGA的NSQ-NSCLC患者,以EGFR突变为例,一线EGFR-TKI治疗进展后NSQ-NSCLC患者的中位PFS也仅为4.4~5.4个月[6,7]。因此,无论是伴还是不伴AGA的晚期NSCLC患者,在接受指南推荐的标准治疗方案并进展后,仍面临较为有限的生存获益。如何进一步提高既往经治NSCLC患者的生存期,是当前临床亟需思考和解决的问题。
既往研究显示,64%~75%的NSCLC患者存在TROP2高表达,且TROP2高表达与患者生存期缩短及不良预后密切相关[8],这为TROP2成为NSCLC治疗的靶点提供了可能。目前,Dato-DXd作为TROP2 ADC的代表药物,广泛布局NSCLC,评估其用于全人群经治NSCLC(鳞癌、非鳞癌)疗效和安全性的TROPION-Lung01研究亦为首个且目前唯一取得阳性结果的Ⅲ期临床试验。凭借优异的疗效和安全性数据,Dato-DXd有望逆转晚期经治患者未尽之需。
再添新证
NSQ-NSCLC患者或成Dato-DXd治疗优势人群
TROPION-Lung01研究是一项全球性、随机、多中心、开放标签的Ⅲ期临床试验,旨在评估Dato-DXd (6mg/kg Q3W) 对比多西他赛 (75mg/m2 Q3W) 在既往至少接受过一次治疗、伴或不伴有可靶向AGA的局部晚期或转移性NSCLC患者的有效性和安全性[9]。
第一阶段和第二阶段研究成果显示,在意向治疗人群(ITT)中,Dato-DXd组较多西他赛组患者显示出具有统计学意义的中位PFS获益,分别为4.4个月和3.7个月,降低疾病进展或死亡风险25%,两组确认的客观缓解率(ORR)分别为26.4%和12.8%,中位缓解持续时间(DOR)分别为7.1个月和5.6个月。无论患者是否存在AGA,都能从Dato-DXd单药治疗中取得PFS获益,且Dato-DXd组显著延长伴有AGA患者的中位PFS,达6.8个月,较多西他赛组绝对延长4.2个月,降低疾病进展或死亡风险62%,获益更为突出。目前研究中期总生存期(OS)尚未成熟,但已经表现出Dato-DXd治疗获益的趋势。研究者认为,以上治疗效果可能更主要归因于Dato-DXd对NSQ-NSCLC的治疗作用,继而启发研究者开展了第三阶段随访分析。
此次ELCC大会公布了第三阶段分析结果[10]。研究对不同组织学类型的预设亚组的PFS和OS进行分析;其中NSQ-NSCLC患者的安全性属于事后分析;患者PFS和抗肿瘤反应通过盲态独立中心审查(BICR)的RECIST 1.1标准进行评估。
在分配到Dato-DXd组的299名患者和分配到多西他赛组的305名患者中,各有234名患者的组织学类型为NSQ-NSCLC。截至2023年3月29日,Dato-DXd组和多西他赛组的中位随访时间分别为12.9个月和12.7个月,结果显示,Dato-DXd组较多西他赛组显著提升患者的中位PFS,分别为5.5个月和3.6个月,降低疾病进展或死亡风险达37% (HR=0.63, 95%CI: 0.51-0.79),两组6个月PFS率分别为46.6%和28.2% (图1)。
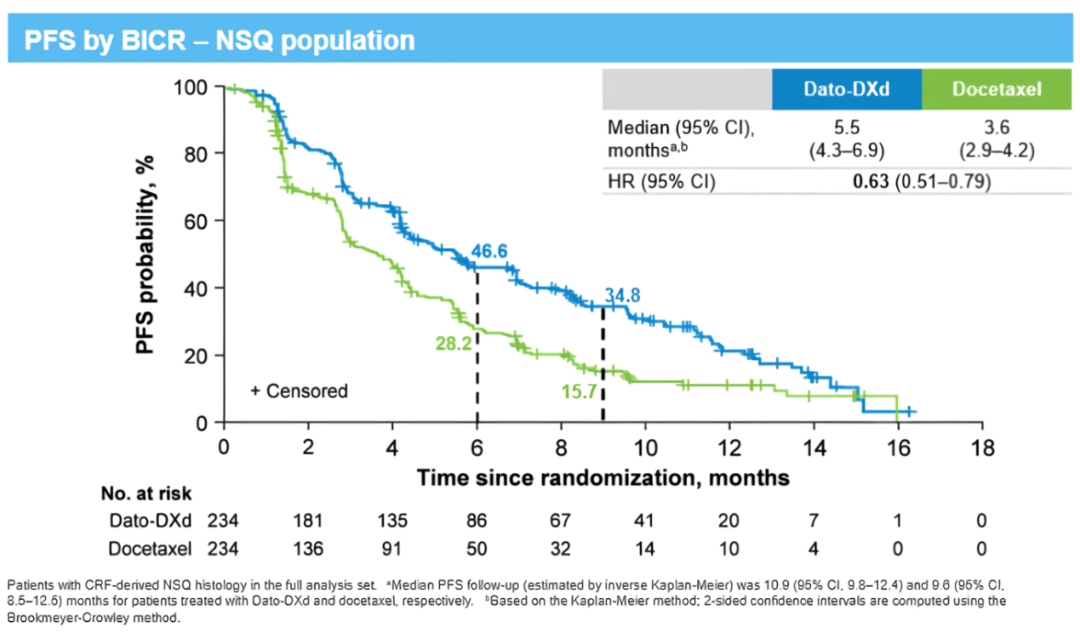
图1.TROPION-Lung01研究
NSQ-NSCLC亚组PFS结果
在NSQ-NSCLC亚组中,研究的另一主要终点OS数据尚未成熟,但Dato-DXd组较多西他赛组表现出令人鼓舞的OS获益趋势,中位OS分别为13.4个月和11.4个月 (HR=0.79, 95%CI: 0.60-1.02)。疾病缓解方面,Dato-DXd组确认的ORR达31%,较多西他赛组提升18%,其中,Dato-DXd组有4例患者出现了完全缓解 (CR)(占2%),69例患者出现了部分缓解 (PR)(占30%),而多西他赛组无CR患者,且仅30例患者PR (占13%)。与多西他赛组相比,Dato-DXd组的DOR提升2.1个月,长达7.7个月,疾病控制率 (DCR) 提升19%,高达80%,较多西他赛组显示了持久的抗肿瘤活性 (图2)。
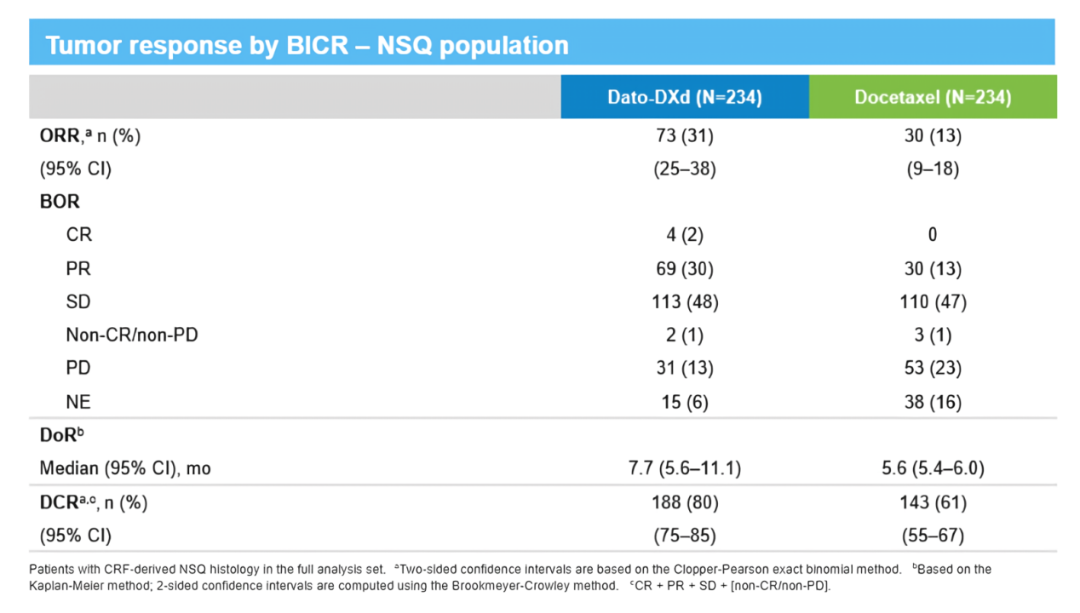
图2.TROPION-Lung01研究
NSQ-NSCLC亚组肿瘤应答结果
安全性方面,在NSQ-NSCLC亚组中,Dato-DXd组和多西他赛组发生任何级别治疗相关不良事件(TRAEs)的患者比例均为88%,且Dato-DXd组在出现了3级及以上不良事件、因TRAEs需要减少剂量以及因TRAEs停止治疗方面的患者比例均低于多西他赛组,分别为22%和41%、21%和30%和9%和12%。
由此亚组更新数据可见,与多西他赛相比,Dato-DXd治疗NSQ-NSCLC患者展示显著获益的PFS改善以及良好的安全性。相信随着随访时间的持续,未来最终OS数据的公布还将为我们带来更多的临床参考和指导。
优化结构Dato-DXd兼具卓越疗效与良好安全性
基于正常组织细胞亦可表达TROP2 靶点的特性,如何通过优化结构设计获得兼具疗效和安全性的ADC成为研发难点。而Dato-DXd兼具着优化的抗体、稳定的特异性四肽可裂解连接子、高活性载药Dxd以及经过疗效和安全性评估的药物抗体比(DAR)等独特优势,为其卓越疗效和良好安全性打下坚实基础。
抗体对于ADC药物与靶向抗原间的特异性结合至关重要。Dato-DXd等多种ADC类药物均采用人源化IgG1抗体,但不同人源化IgG1抗体的解离常数(KD)不同,KD值越高,亲和力越低,则提示药物毒性越低[11]。Dato-DXd的抗体为MAAP-9001a,具有较高的KD值,有效降低药物在正常组织中的毒性[12],提升Dato-DXd的安全性。
连接子在抗体和有效载荷之间扮演着“桥梁”的角色。Dato-DXd采用优化的四肽可裂解连接子在减少ADC的疏水性和聚集性、增加其稳定性的同时,可降低清除率,在血液循环中呈高度稳定状态,有效避免载药提前释放;且仅能被肿瘤细胞内的溶酶体蛋白酶特异性识别并切割,实现在肿瘤细胞内精准释放载药,有效降低脱靶毒性[13]。
DXd作为高活性载荷具有独特的作用机制和强大的抗肿瘤活性,是Dato-DXd的制胜关键。首先,DXd具有很强的渗透细胞膜的能力,在杀伤吞入ADC的肿瘤细胞之后,还能够杀死附近的肿瘤细胞,产生“旁观者效应”。其次,DXd的活性是SN-38(伊立替康活性代谢产物)的10倍,是常见化疗药物的100~1000倍[14],可有效干扰DNA复制、重组和基因表达。此外,根据临床前试验的安全性数据,Dato-DXd调整DAR为4,扩大治疗窗的同时进一步提升安全性[15-16]。
基于此,专业的技术支持、独特的作用机制和优化的结构设计实现了Dato-DXd安全性、疗效双优。随着Dato-DXd在肺癌领域的全面布局,Dato-DXd将成为肺癌领域中极具治疗前景的TROP2 ADC。
未来可期
TROPION-Lung系列有望惠及更多肺癌患者
目前,Dato-DXd凭借TROPION-Lung01研究在经治局晚期或转移性NSCLC展示卓越疗效的同时,其在联合治疗模式方面亦表现出可观的治疗潜力。
TROPION-Lung02是首个探索Dato-DXd联合免疫疗法(帕博利珠单抗)±铂类化疗方案治疗晚期NSCLC的临床研究,结果显示[17],无论入组患者既往是否接受过治疗,Dato-DXd联合帕博利珠单抗的二联方案的ORR为38%,DCR为84%,中位PFS为8.3个月;Dato-DXd联合帕博利珠单抗联合化疗的三联方案,ORR为49%,DCR为87%,中位PFS为7.8个月。TROPION-Lung04研究结果则提示[18],对于初治或放疗后出现进展或既往接受过一线化疗且未使用过免疫检查点抑制剂的晚期/转移性NSCLC患者,Dato-DXd联合度伐利尤单抗的二联方案的ORR为50.0%,DCR为92.9%;Dato-DXd联合度伐利尤单抗和化疗的三联方案的ORR达到76.9%,DCR为92.3%,且所有PD-L1表达水平的患者中均观察到肿瘤缓解,三联疗法的缓解率普遍高于双联疗法。
此外,目前正在进行的TROPION-Lung07、TROPION-Lung08及AVANZAR研究则是TROP2 ADC联合治疗挑战肺癌一线标准治疗的更深入、更精准的探索[19-21]。TROPION-Lung07将目光聚集到Dato-DXd+免疫检查点抑制剂±化疗在PD-L1<50%的晚期或转移性NSCLC患者中的疗效与安全性;TROPION-Lung08研究将进一步评估Dato-DXd+帕博利珠单抗对比帕博利珠单抗单药一线治疗驱动基因阴性PD-L1 TPS≥50%晚期或转移性NSCLC的疗效和安全性。AVANZAR研究则将评估Dato-DXd与度伐利尤单抗和卡铂联用作为一线治疗用于局部晚期/转移性NSCLC的疗效及安全性。
可以看到,无论是从后线到一线,抑或是从单药到联合,Dato-DXd在治疗晚期NSCLC方面均表现出充满希望的治疗前景。相信随着未来更多随访数据及探索性研究结果的公布,Dato-DXd治疗晚期NSCLC患者势必将表现出更大的治疗价值与潜力,从而惠及更多肺癌患者。
参考文献:
1.Rotow J, et al. Nat Rev Cancer, 2017,17(11):637-658.
2.Meador CB, et al. Pharmacol Ther, 2020,210:107522.
3.Wu SG, et al. Mol Cancer, 2018,17(1):38.
4.《CSCO非小细胞肺癌诊疗指南2023》.
5.Yang JC, et al. 2023 ASCO: LBA9000.
6.Wu YL, et al. J ThoracOnco1,2019,14(5):867-875.
7.Ding J, et al. Expert Rev Anticancer Ther. 2023 Feb;23(2):187-198.
8.Liu X, et al. Pharmacol Ther, 2022,239:108296.
9.MJ. Ahn, et al. 2023 ESMO: LBA12.
10.https://cslide.ctimeetingtech.com/elcc24hybrid/attendee/confcal_1/presentation/list?q=59p
11. Robert A. Copeland. Enzymes: A Practical Introduction to Structure, Mechanism, and Data Analysis. Chapter.04 Protein-ligand binding equilibria .
12.Shimizu T,et al. J Clin Oncol. Published online June 16, 2023.
13.Ogitani Y, et al. Clin Cancer Res, 2016, 22(20):5097-5108.
14.Nakada T, et al. Chem Pharm Bull (Tokyo). 2019;67(3):173-185.
15.Okajima D, et al. Mol Cancer Ther, 2021,20(12):2329-2340.
16.Liu X, et al. Pharmacol Ther. 2022 Nov;239:108296.
17.Goto Y, et al. 2023 ASCO. Abstract 9004.
18.Papadopoulos KP, et al.2023 WCLC. OA05.06D.
19.C. Zhou, et al. Journal of Thoracic Oncology,2023,18(11S):S327-S328.
20.I. Okamoto, et al. Annals of Oncology,2023,34(S2):S847-S848.
21.C. Aggarwal, et al. Journal of Thoracic Oncology,2023,18(11S):S305-S306. |
|