|
|
作者:肿瘤资讯
整理:肿瘤资讯
来源:肿瘤资讯
以下内容仅供中国大陆地区执业的医学药学专业人士阅读参考,如您非前述专业人士,请离开本页面
病例点评:北京协和医院 基本外科 康维明教授
病例整理:北京协和医院 郑紫城博士、刘冠墨博士
本文介绍一例胃GIST患者,初诊肿瘤直径大于10cm,且与胰腺、脾脏关系密切,直接手术联合脏器切除风险较大。伊马替尼用药14个月后,肿瘤缩小不明显,未达到手术要求。后换用瑞派替尼治疗近8个月,安全性良好,肿瘤缩小达26%,病灶与胰腺组织、脾动脉分界清晰,最终实施完整的R0手术切除,并保留脾脏。本案例提供了有力的证据,支持瑞派替尼在术前新辅助治疗中的潜在价值,为临床实践提供了新的思路。

专家点评
点击边框调出视频工具条
康维明教授点评
病例简介
基本情况
患者2021年体检发现胃脾间隙肿物。2021年12月就诊于当地医院,CT提示左侧脾、胃、胰腺间隙不规则软组织密度影,大小12.8cm*9cm,局部与胃底壁、左肾上腺分界欠清,与胰腺分界欠清,脾动脉包绕。明确肿物性质行肿物穿刺活检术,病理提示“胃肠间质瘤”,基因检测报告显示KIT外显子11 V559D突变。
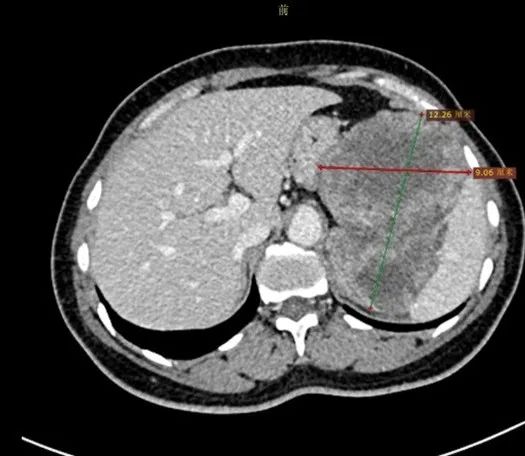
2021年12月CT(最大截面)
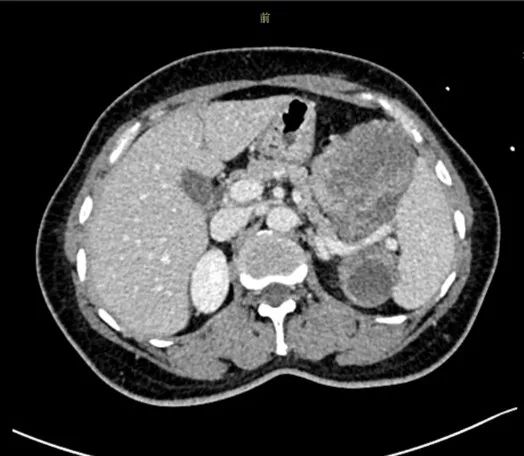
2021年12月CT 胰腺脾脏关系
治疗经过
伊马替尼新辅助治疗
因病灶与胰腺、脾血管关系密切,直接手术联合脏器切除风险较大。2022年1月当地医院给予伊马替尼400mg QD治疗。伊马替尼服药期间不良反应较为突出,包括持续恶心呕吐、水肿、全身苍白及贫血2级。
治疗期间定期复查腹部CT。2023年3月,伊马替尼用药14个月,患者复查腹部CT提示“脾胃间隙巨大肿块,病灶范围较前变化不明显,大小约11.5*7.1cm,伴增强,病灶与胰腺分界稍清,与脾脏、胃大弯侧胃壁关系密切,脾动脉包绕,可见供血血管。
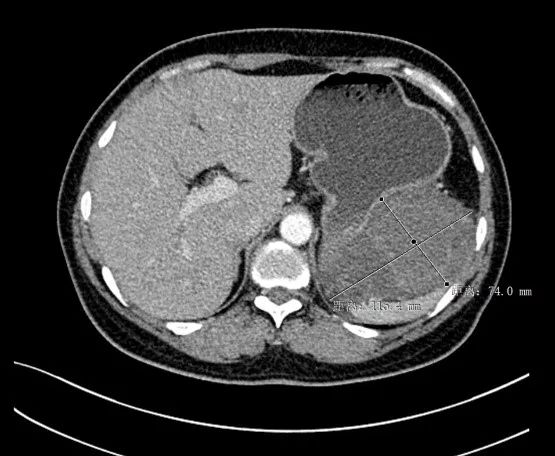
2023年3月CT(最大截面)
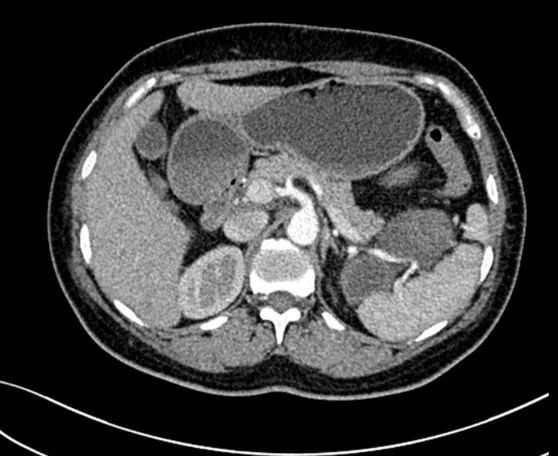
2023年3月CT 胰腺脾脏关系
瑞派替尼新辅助治疗
2023年3月就诊于我院,评估手术,切除范围较大,且可能涉及联合脏器切除,建议选择有效的TKI治疗以进一步缩小肿瘤,经与患者充分沟通知情同意,患者于2023年4月23日开始服用瑞派替尼150mg QD治疗。换用瑞派替尼之后,伊马替尼服药期间出现的贫血、恶心呕吐,水肿等不良反应消失,出现脱发、肌痛、牙龈出血不良反应,均为1-2级。血细胞指标、肝肾功能正常。
2023年9月22日复查腹盆增强CT+胃重建提示“脾胃间隙可见囊实性密度占位,似见包膜,占位形态不规则,局部凸向胃腔,胃腔粘膜面基本完整,病灶与胰腺分界清,与脾动脉分界清晰,较大截面约10cm*5.7cm*6.6cm,增强扫描实性部分呈轻度强化,囊性低密度部分未见强化。建议患者准备手术。
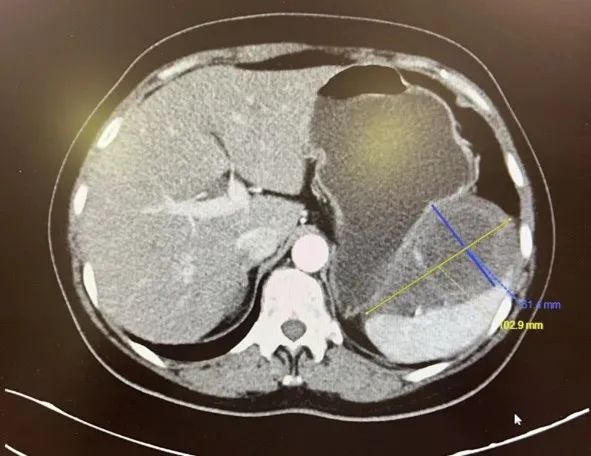
2023年9月CT(最大截面)
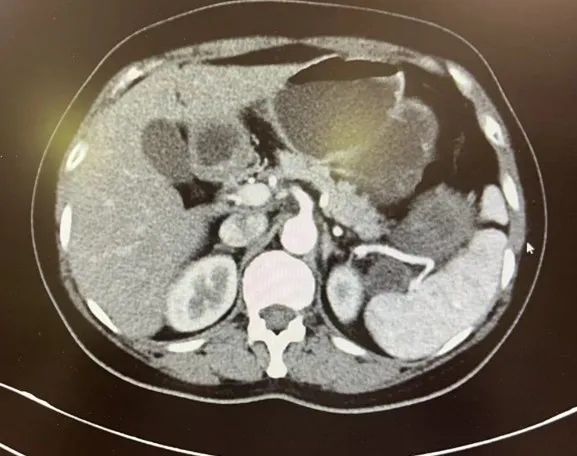
2023年9月CT 胰腺脾脏关系
手术
术前检查:2023年12月,瑞派替尼用药8个月,CT平扫显示,脾胃间隙可见囊实性密度占位,似见包膜,占位形态不规则,局部凸向胃腔。超声内镜显示,胃体后壁见直径约7.9*6.7cm低回声占位,内部可见多发无回声区,病灶紧邻胃壁,局部与固有肌层分界欠清。
2023年12月19日手术,手术前停药1周。行“腹腔镜胃部分切除术;腹腔探查术”,探查发现胃壁肿物位于胃底大弯侧后壁贲门下方,肿物大小约8*6cm,大部分突出胃轮廓之外,距离贲门约5cm,紧靠脾门及脾血管,与术前胃镜及CT等检查结果一致。肿物与脾脏及后腹膜粘连紧密,小心分离粘连,逐步将肿物与脾脏及脾血管分开。使用直线切割闭合器分次切下肿瘤周围胃壁全层,切缘距离肿物根部超过2cm,完整切除肿物。手术顺利,术中出血约400ml,回输患者术前保留的400ml自体血及200ml异体血浆。患者恢复良好,手术第二天拔出腹腔引流管,伤口愈合良好。2023年12月27日出院。
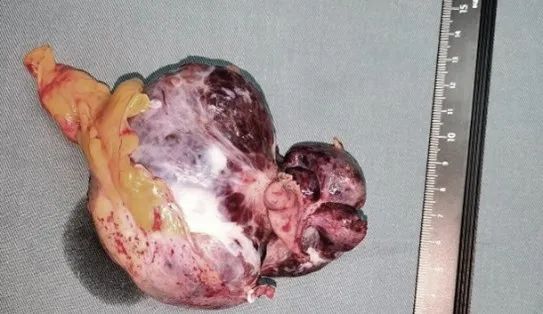
2023年12月19日手术样本
术后病理显示,胃肠间质瘤,大小8.5*6cm,核分裂像3/50HPF,伴退变坏死,未累及胃粘膜;肿瘤表面被包膜,局部附胃壁组织,面积2.5*2cm,病理检查为纤维脂肪组织。术后基因检测显示KIT 11 V559D突变。
肿瘤大小变化
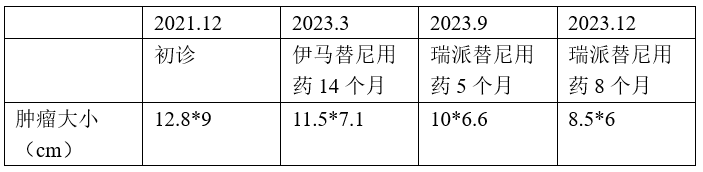
专家点评
康维明教授:
手术是原发可切除胃肠间质瘤患者的首选治疗,特殊情况下,需考虑新辅助治疗。2024版NCCN胃肠间质瘤诊疗指南指出,对于某些解剖部位(例如,直肠、食管和食管胃交界处、十二指肠)的局晚期GIST,如果需要多脏器切除才能切除所有大体肿瘤,或者患者存在显著的合并症而不适合手术,则应考虑对基因型敏感疾病进行新辅助治疗1。2023版CSCO胃肠间质瘤诊疗指南也指出,术前评估预期肿瘤难以达到R0切除、需联合脏器切除、可完整切除但手术风险较大者,应考虑新辅助治疗。新辅助治疗可提高局限进展期GIST患者的手术切除率,保存器官功能2。多项研究也表明,新辅助治疗可以给局晚期GIST患者带来长期生存获益3-5。各项研究提示,伊马替尼新辅助治疗,ORR率为43%-80%,R0切除率为36%-100%3-10,提示仍存在伊马替尼不敏感或疗效有限的患者,难以满足手术需求。
同时,伊马替尼新辅助治疗的时间及手术时机的选择也是临床关注的重点。NCCN胃肠间质瘤诊疗指南指出,最大缓解可能需要治疗6个月或更长时间才能达到。一旦达到最大缓解,则考虑手术切除。CSCO胃肠间质瘤诊疗指南也指出,在肿瘤不再退缩或者达到手术要求后,再行手术切除。B2222研究11和EORTC12研究中,伊马替尼的至客观缓解中位时间分别为13周和107天,目前临床一般采用的新辅助治疗时间多为6-12个月。本例患者伊马替尼已治疗14个月,肿瘤从12.8cm缩小至11.5cm,缩瘤效果不理想,病灶与脾脏、胃大弯侧胃壁关系密切,手术仍具有较大风险。因此,亟需其它治疗方案,以达到更好的缩瘤及完整手术切除的目的。
瑞派替尼是新型的开关控制抑制剂,可广泛的抑制KIT/PDGFRA各种原发和继发突变类型13,瑞派替尼在晚期胃肠间质瘤二线(入组伊马替尼治疗进展或不耐受的患者)全球Ⅲ期INTRIGUE研究显示,瑞派替尼在全人群及KIT外显子11突变的人群中,ORR分别达到了22%和24%。同时,中国二线研究中14,也观察到瑞派替尼具有高缓解率的优势,在全人群和KIT外显子11突变的人群中, ORR分别达到30%和37%。因此,在伊马替尼治疗进展或者不耐受的患者中,瑞派替尼提供了进一步缩瘤的机会。目前,瑞派替尼在新辅助治疗中的应用尚未得到充分探索。本病例中,瑞派替尼使用近8个月,肿瘤从11.5cm缩小至8.5cm,肿瘤缩小达26%,病灶与胰腺组织、脾动脉分界清晰,最终实施完整的R0手术切除,并保留脾脏。
手术的安全性是外科医生必须考虑的重要因素。手术并发症是手术治疗必须要考虑的重要问题,而药物治疗可能增加围手术期并发症风险。国内外多项研究表明,瑞派替尼安全性和耐受性良好,不良反应多数为1~2级,用药过程中治疗相关AE导致的剂量调整比例较低15, 16。良好的药物安全性为降低手术风险提供一定保障。本例患者在伊马替尼使用期间水肿、恶心呕吐等不良反应明显,换用瑞派替尼之后患者自诉不良反应明显改善。且瑞派替尼新辅助治疗使用后,术前停药1周,出血整体可控。整体治疗安全性良好,术后未发生手术并发症。
本案例表明,利用瑞派替尼作为新辅助治疗可被视为伊马替尼新辅助治疗疗效欠佳的胃肠间质瘤患者的可行选择。本案例提供了有力的证据,支持瑞派替尼在术前新辅助治疗中的潜在价值,为临床实践提供了新的思路。
参考文献:
1. NCCN clinical practice guidelines in Oncology: Gastrointestinal Stromal Tumors (GISTs)((Version 1.2024). 2024.
2. 中国临床肿瘤学会指南工作委员会组织编写. 中国临床肿瘤学会(CSCO)胃肠间质瘤诊疗指南. 人民卫生出版社 2023.
3. Blesius A, Cassier PA, Bertucci F et al. Neoadjuvant imatinib in patients with locally advanced non metastatic GIST in the prospective BFR14 trial. BMC Cancer 2011; 11: 72.
4. Rutkowski P, Gronchi A, Hohenberger P et al. Neoadjuvant imatinib in locally advanced gastrointestinal stromal tumors (GIST): the EORTC STBSG experience. Ann Surg Oncol 2013; 20 (9): 2937-2943.
5. Tielen R, Verhoef C, van Coevorden F et al. Surgical treatment of locally advanced, non-metastatic, gastrointestinal stromal tumours after treatment with imatinib. Eur J Surg Oncol 2013; 39 (2): 150-155.
6. Fiore M, Palassini E, Fumagalli E et al. Preoperative imatinib mesylate for unresectable or locally advanced primary gastrointestinal stromal tumors (GIST). Eur J Surg Oncol 2009; 35 (7): 739-745.
7. Kurokawa Y, Yang HK, Cho H et al. Phase II study of neoadjuvant imatinib in large gastrointestinal stromal tumours of the stomach. Br J Cancer 2017; 117 (1): 25-32.
8. Reichardt P. The Story of Imatinib in GIST - a Journey through the Development of a Targeted Therapy. Oncol Res Treat 2018; 41 (7-8): 472-477.
9. Eisenberg BL, Harris J, Blanke CD et al. Phase II trial of neoadjuvant/adjuvant imatinib mesylate (IM) for advanced primary and metastatic/recurrent operable gastrointestinal stromal tumor (GIST): early results of RTOG 0132/ACRIN 6665. J Surg Oncol 2009; 99 (1): 42-47.
10. Wang D, Zhang Q, Blanke CD et al. Phase II trial of neoadjuvant/adjuvant imatinib mesylate for advanced primary and metastatic/recurrent operable gastrointestinal stromal tumors: long-term follow-up results of Radiation Therapy Oncology Group 0132. Ann Surg Oncol 2012; 19 (4): 1074-1080.
11. Demetri GD, von Mehren M, Blanke CD et al. Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med 2002; 347 (7): 472-480.
12. Verweij J, Casali PG, Zalcberg J et al. Progression-free survival in gastrointestinal stromal tumours with high-dose imatinib: randomised trial. Lancet 2004; 364 (9440): 1127-1134.
13. Smith BD, Kaufman MD, Lu WP et al. Ripretinib (DCC-2618) Is a Switch Control Kinase Inhibitor of a Broad Spectrum of Oncogenic and Drug-Resistant KIT and PDGFRA Variants. Cancer Cell 2019; 35 (5): 738-751.e739.
14. Li J, Zhang J, Zhang Y et al. Efficacy and safety of ripretinib vs. sunitinib in patients with advanced gastrointestinal stromal tumor previously treated with imatinib: A phase 2, multicenter, randomized, open-label study in China. Eur J Cancer 2024; 196: 113439.
15. Blay JY, Serrano C, Heinrich MC et al. Ripretinib in patients with advanced gastrointestinal stromal tumours (INVICTUS): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 2020; 21 (7): 923-934.
16. Li J, Cai S, Zhou Y et al. Efficacy and Safety of Ripretinib in Chinese Patients with Advanced Gastrointestinal Stromal Tumors as a Fourth- or Later-Line Therapy: A Multicenter, Single-Arm, Open-Label Phase II Study. Clin Cancer Res 2022; 28 (16): 3425-3432.
*以上信息涉及尚未在中国获批的产品/适应症。此信息仅作信息分享用途,不应被理解为这些产品/适应症在中国获批或注册。
责任编辑:肿瘤资讯-Marie
排版编辑:肿瘤资讯-CYX
版权声明
本文专供医学专业人士参考,未经著作人许可,不可出版发行。同时,欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。
|
|