马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
在 III 期非小细胞肺癌患者中,若已明确存在 EGFR、ALK、ROS1、KRAS 等可靶向驱动基因突变,ctDNA-MRD(分子残留病灶)能否在真实世界路径里实现“可执行、可重复、可解释”的复发风险预警,一直是临床关心的问题。国内多中心协作开展的 DRIVE 研究(Prospective Observational Study on Dynamic Monitoring of Residual DrIVer Mutations for DiseasE Recurrence in Stage III NSCLC,DRIVE Study,NCT06443684)尝试给出一条更可落地的解法:相较于依赖肿瘤组织定制的大规模个体化位点追踪,该研究以驱动突变为核心锚点,采用更聚焦的检测策略进行术后与随访期动态监测,探索在保证风险分层能力的同时,降低流程复杂度、提升可及性。
DRIVE 为前瞻性观察性多中心研究,由上海市胸科医院陆舜教授牵头,全国 14 家中心共同参与。研究入组 2022–2025 年间肿瘤组织确认携带至少 1 个驱动突变(EGFR、ALK、ROS1、KRAS、BRAF、MET、RET、HER2、NRAS、PIK3CA),且未接受系统性抗肿瘤治疗的可手术 III 期 NSCLC 患者;在最终筛选的 198 例患者中,EGFR 突变占 62%(123/198),KRAS 突变占 16%(32/198),ALK 突变占 7%(13/198)。研究在治疗前、根治术后或内科治疗后及随访过程中采集外周血样本并开展 ctDNA 检测,以评估聚焦驱动突变的 MRD 策略在术后复发风险监测与全病程管理中的价值。
在 2025 年 ESMO Asia 期间,上海市胸科医院李子明教授于胸部肿瘤 Mini Oral 专场公布了该研究的首次分析结果。作为国内多中心联合完成的前瞻性探索性工作,DRIVE 的阶段性数据在国际学术平台集中呈现了中国团队在“聚焦驱动突变 MRD 监测”方面的实践经验与临床价值,并引发了与会同行对其在围手术期管理与随访策略中应用前景的进一步讨论。
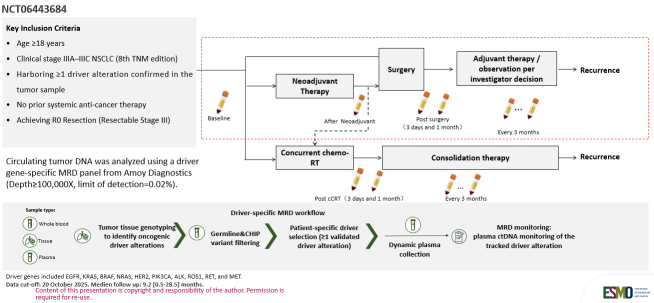
图1 研究设计
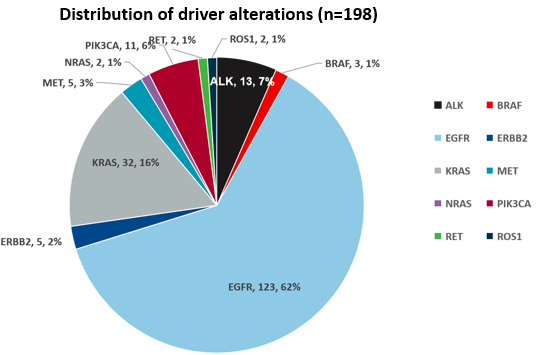
图2 入组患者驱动基因分布
此次会议汇报结果中,研究团队得出了几个重要结论:
01 已发表研究二次分析:聚焦驱动突变的 MRD 方案在预后分层能力上与定制化 tumor-informed 或大 panel 方案总体相当,部分队列中呈现更优的风险区分度。
在驱动突变 NSCLC 人群中,仅围绕已知驱动突变开展 ctDNA 监测,已能提供足够稳定且可解释的 MRD 风险分层依据。该研究对三项既往可手术肺癌 MRD 研究中组织确认“驱动基因阳性”亚群进行了二次分析,覆盖 1 个 WES + 约 50 位点 tumor-informed 队列(62 例驱动阳性),以及 2 个固定大 panel 队列(139 基因 panel:49 例驱动阳性;127 基因 panel:25 例驱动阳性)。在不改变原始数据的前提下,我们仅基于患者已知驱动突变的 ctDNA 阴阳性,重新定义“驱动 MRD”,并分别与原研究采用的 MRD 指标比较其对术后复发风险的区分能力:在 tumor-informed 队列中,驱动 MRD 与原 MRD 的 HR 分别为 20.12 与 5.69;在 139 基因 panel 队列中,两者 HR 均为 7.87;在 127 基因 panel 队列中,驱动 MRD 的 HR 为 6.90,而原 MRD 为 3.63。
整体趋势提示:在驱动阳性、可手术肺癌中,仅基于驱动突变的 MRD 定义并未降低对术后复发风险的辨识能力,从而为“聚焦驱动”的策略提供了更现实的可行性依据。

图3. 三项术后MRD研究中驱动突变患者数据二次分析结果
02 长期随访患者中,持续阴性患者复发极少,阳性/转阳者复发事件明显集中
在术后动态监测中,持续 ctDNA 阴性的患者复发率更低;相较 ctDNA 阴性者,ctDNA 阳性患者的一年 DFS 为 60.6% vs 92.7%,中位 DFS(mDFS)为 13.4 个月 vs 未达到(NR),复发风险显著升高(HR=8.72,P<0.001)。在 EGFR 突变亚组中,这一关联更为突出:ctDNA 阳性 vs 阴性患者的一年 DFS 为 77.8% vs 97.9%,mDFS 为 23.1 个月 vs NR,HR=29.72(P<0.001)。
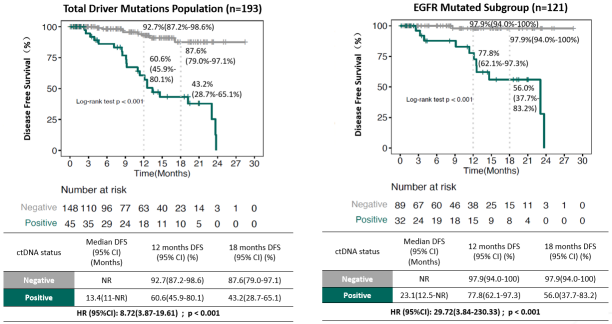
图4. 术后驱动基因突变ctDNA MRD状态与患者DFS相关性
03 关键术后节点:术后 3 天/1 个月的 ctDNA 状态同样具有明确的预后指示意义
在整体人群中,术后第 3 天 ctDNA 阳性患者的预后明显劣于 ctDNA 阴性者:一年 DFS 率分别为 63.4% 与 90.7%,中位 DFS 为 12.6 个月 vs 未达到(NR),复发风险增加(HR=5.59,P<0.001)。术后约 1 个月时同样呈现一致趋势,ctDNA 阳性 vs 阴性患者的一年 DFS 率为 67.2% vs 94.8%,中位 DFS 为 19.2 个月 vs 23.8 个月,HR=5.81(P<0.001)。
在 EGFR 突变亚组中,landmark 节点的区分度更为显著:术后第 3 天 ctDNA 阳性患者的一年 DFS 率为 80.2%,低于阴性者的 96.3%,中位 DFS 为 12.6 个月 vs NR,HR=13.44(P<0.001);术后约 1 个月时,ctDNA 阳性 vs 阴性患者一年 DFS 率为 75.2% vs 100%,两组中位 DFS 均未达到,但风险差异仍然显著(HR=9.98,P<0.001)。
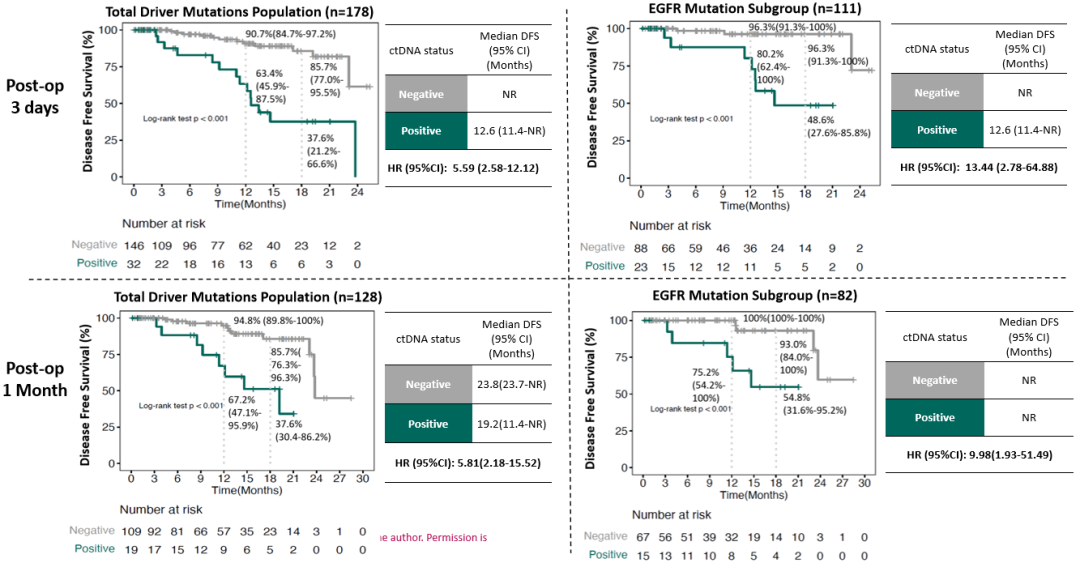
图5. 关键时间点驱动基因突变ctDNA状态与患者DFS相关性
04 在所有驱动基因突变人群中,动态ctDNA监测较影像学更早提示进展,EGFR 亚组提前 11.3 个月
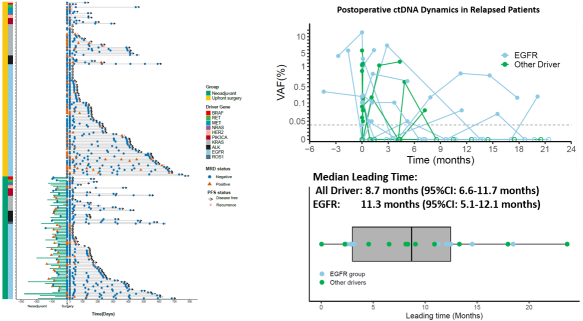
图6. 动态ctDNA监测先于影像学预测患者复发
点评 来自香港中文大学威尔士亲王医院的龙浩锋教授(Hubert Ho Fung Loong)在点评环节同样也指出,ctDNA 用于 MRD 检测的临床价值已逐步明确。与此同时,EGFR、KRAS 等驱动突变多为肺癌发生发展过程中的早期事件,并在肿瘤演进中相对稳定保留,这也为“聚焦驱动突变”作为 MRD 监测锚点提供了生物学基础。基于此,本研究采用“聚焦驱动突变”的检测策略,契合亚洲人群可靶向驱动突变比例较高的疾病特征,有望在保证信息量的同时进一步缩短检测周转时间、降低成本,并在一定程度上减少克隆性造血(CHIP)带来的干扰,从而提升 MRD 在真实世界中的可及性与可推广性。就本次汇报结果而言,无论是在术后纵向随访的动态监测框架下,还是在术后 3 天与术后 1 个月等关键 landmark 时间点,驱动 ctDNA 阳性均与更差的 DFS 显著相关,整体趋势与既往 MRD 研究方向一致、具有可解释性。龙教授也表示,随着随访时间进一步延长、事件持续累积,这项研究有望为驱动基因阳性可手术肺癌人群提供更高等级、可用于指导临床管理的 MRD 证据支持。
结果与展望 III 期非小细胞肺癌复发风险整体偏高,围手术期治疗路径复杂,且患者间异质性显著。基于此,仅依赖 TNM 分期与影像随访往往难以满足精细化管理需求,引入更敏感的风险分层工具具有现实必要性。DRIVE研究(NCT06443684)聚焦其中明确携带驱动基因突变的可手术患者,采用更简化、聚焦的“驱动突变 ctDNA-MRD”策略,评估术后 3 天、术后 1 个月等关键时间点及持续动态监测能否提供具有临床意义的风险信息。结果提示:长期随访中持续 ctDNA 阴性的患者复发事件极少,而持续阳性或随访过程中转阳者复发风险显著升高;此外,术后 3 天与术后 1 个月的 ctDNA 状态同样具有明确的预后分层价值。值得关注的是,ctDNA 动态监测较影像学可提前中位 8.7 个月提示疾病进展,在 EGFR 突变亚组中提前可达 11.3 个月。总体而言,上述发现为术后个体化随访节奏制定与精准管理提供了可参考的初步依据;而该策略能否进一步转化为 III 期患者长期生存获益,仍需更长随访及后续研究持续验证。 |