马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
文献 今日分享一篇发表在Clinical Lung Cancer杂志2024年的文献,通讯作者是来自美国芝加哥大学医学中心的 Jessica Donington教授。


前言 肺癌是美国癌症相关死亡的首要原因,占2022年所有癌症死亡的21%。其中85%的病例为非小细胞肺癌(NSCLC)。非小细胞肺癌的治疗策略取决于临床分期和患者的身体状况。对于Ⅰ期疾病,推荐单独进行手术切除,而对于Ⅱ-Ⅲ期疾病,建议采用多模式治疗。对于某些Ⅱ期和N2+的ⅢA期NSCLC患者,推荐使用新辅助全身治疗或化疗放疗,随后进行手术和辅助铂类双药化疗,这是根据NCCN肿瘤学临床实践指南的建议。对于N2阳性ⅢA期和部分ⅡB期NSCLC患者,可切除性通常由肿瘤体积和淋巴结受累程度决定。对于被认为可切除的患者,标准治疗是新辅助化疗(伴或不伴胸部放疗),随后进行手术切除。然而,40%-70%的患者在接受初始治疗后会出现肿瘤复发。免疫检查点抑制剂扩展了新辅助治疗的选择。这些药物利用抗程序性死亡1(PD-1)和程序性死亡配体1(PD-L1)的肿瘤相互作用,彻底改变了晚期疾病患者的治疗,并在辅助治疗中显示出疗效和安全性。PD-1抗体纳武利尤单抗联合铂类化疗是美国食品药品监督管理局(FDA)批准用于NSCLC新辅助治疗的免疫疗法之一。此外, CheckMate 77T研究的最新结果显示,纳武利尤单抗联合化疗作为新辅助治疗,随后进行辅助纳武利尤单抗治疗,可显著改善可切除NSCLC患者的无事件生存期(EFS)。基于 KEYNOTE-671试验中接受新辅助 帕博利珠单抗治疗的患者显著的临床获益,FDA批准了帕博利珠单抗联合含铂化疗作为可切除(肿瘤≥4cm或淋巴结阳性)NSCLC的新辅助治疗。另一种类似药物度伐利尤单抗联合化疗也在 AEGEAN试验中被评估用于可切除NSCLC的新辅助治疗。 鉴于可切除NSCLC治疗格局的不断发展,更好地了解临床实践中患者的治疗模式和预后结果,有助于明确未满足的治疗需求。在此背景下,本研究考察了美国Ⅱ期、ⅢA期和ⅢB期(N2)NSCLC(AJCC第8版)患者接受新辅助化疗或化疗放疗的治疗模式、生存结果和复发模式。

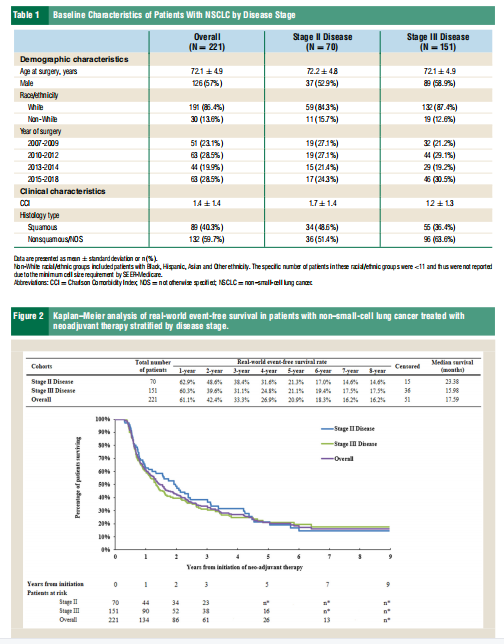
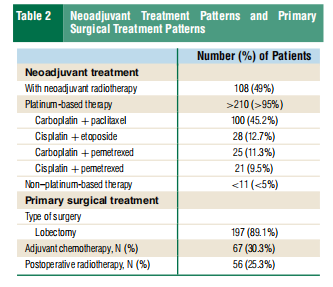
摘要 目的 本研究旨在通过SEER-Medicare数据库(2007-2019)分析接受新辅助治疗的Ⅱ-Ⅲ期可切除非小细胞肺癌(NSCLC)患者的治疗模式、真实世界无事件生存期(rwEFS)和总生存期(OS)。 方法 纳入221例患者(Ⅱ期70例,Ⅲ期151例),中位随访时间为32.7个月。所有患者在手术前均接受了新辅助化疗(51%)或放化疗(49%),其中97%的患者接受了铂类方案,最常见的是卡铂+紫杉醇(45%)。

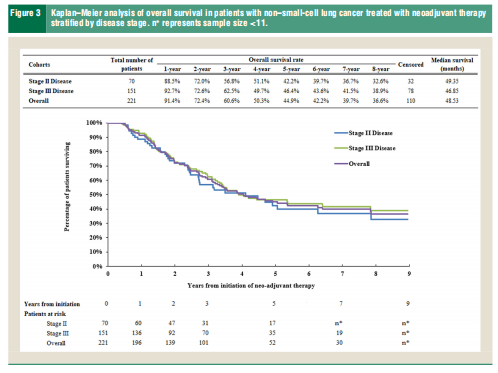
结果 整体人群中,中位rwEFS为17.6个月,5年rwEFS为20.9%;中位OS为48.5个月,5年OS为44.9%。71%的患者在随访期间出现疾病复发,其中28%的复发患者首次复发事件为局部区域复发。
结论 这些结果突显了对更有效新辅助治疗的需求,以改善患者的生存率。

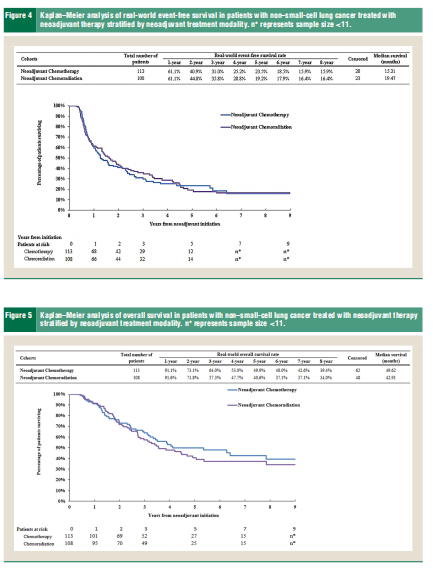
讨论 新辅助化疗可以改善非小细胞肺癌(NSCLC)的术后预后,但关于其在真实世界中的使用策略和有效性信息较少。本研究考察了美国Ⅱ期、ⅢA期和ⅡB期(N2)NSCLC患者接受新辅助化疗或化疗放疗的治疗模式、复发模式以及生存结果(rwEFS和OS)。结果显示,几乎所有患者都接受了铂类方案,近一半患者在新辅助治疗中接受了胸部放疗。整体患者的中位rwEFS为17.6个月,中位OS为48.5个月。在研究期间,超过70%的患者出现肿瘤复发,其中大多数患者的首次复发事件为远处转移。这些发现为美国NSCLC新辅助化疗和化疗放疗的使用和有效性提供了见解,并提示需要更有效的新辅助治疗选择。 化疗通常由铂类药物与吉西他滨、紫杉醇或多西他赛联合组成。本研究中最常用的新辅助化疗方案是卡铂+紫杉醇,这也是在SEER-Medicare数据库中ⅠB期(肿瘤≥4cm)至ⅡB期NSCLC患者辅助治疗中最常见的铂类联合方案。卡铂+紫杉醇与胸部放疗的联合使用在美国社区肿瘤学实践中被广泛使用。新辅助治疗后进行切除在真实世界中的使用并不广泛,这在图1中有所反映。此前的研究也记录了新辅助治疗的使用较少。例如,在一项针对可切除Ⅲ期疾病患者的大型回顾性研究中,只有2.3%的患者接受了新辅助治疗后手术作为一线治疗。此外,Lee等人使用2010-2015年的SEER-Medicare数据评估ⅠA-ⅡB期NSCLC患者的治疗模式,发现约8%的患者接受了新辅助治疗后手术±辅助治疗。 本研究的生存结果与此前发表的真实世界研究一致。在一项针对接受诱导化疗或化疗放疗的Ⅲ期(N2)NSCLC患者的多中心研究中,5年OS率在40%-43%之间,5年无病生存率在29%-30%之间。在另一项针对100个国家的100个中心接受治疗的可切除Ⅲ期疾病患者的大规模回顾性研究中,术前化疗的中位OS为49.8个月,术前同步化疗放疗的中位OS为44.8个月,而中位PFS分别为19.0个月和18.5个月。 需要注意的是,临床试验和真实世界数据并不完全可比,但我们的发现与之前新辅助/围手术期临床研究的结果大致一致。例如,一项针对主要为Ⅰ-Ⅲ期NSCLC患者的15项随机试验的荟萃分析显示,接受新辅助化疗的患者5年OS为45%,5年无复发生存率为36%。本研究报告了类似的5年OS率,但5年EFS率较低,这可能是由于当前研究中疾病复发的定义和患者人群与那些临床试验不同。此外,在支持FDA批准纳武利尤单抗联合铂类双药化疗作为可切除NSCLC新辅助治疗的Ⅲ期 CheckMate 816试验中,化疗组患者的中位EFS为20.8个月,与本研究中的中位rwEFS(17.8个月)相似。值得注意的是,在CheckMate 816中,化疗组中22%的患者也接受了可选的辅助化疗,这与本研究中接受辅助化疗的比例(即30%)接近。最后,在评估可切除NSCLC围手术期帕博利珠单抗的KEYNOTE-671试验中,接受铂类新辅助治疗后手术的患者的中位EFS为17个月。综合来看,现有证据表明,新辅助化疗和化疗放疗的生存率有相当大的提升空间。 接受新辅助化疗的患者与接受新辅助化疗放疗的患者相比,rwEFS相似,OS数值更高。尽管本研究并非旨在比较这两种新辅助治疗模式,且分析具有描述性,但这些发现与现有文献大致一致,因为目前尚无一致证据显示新辅助化疗与新辅助化疗放疗相比具有生存获益。 在早期治疗NSCLC可以改变肿瘤发展进程并延长生存期。有研究表明,免疫治疗在新辅助环境中可能特别有益,因为完整肿瘤上存在的广泛新抗原可以刺激T细胞激活,从而清除微转移。此外,化疗诱导的肿瘤细胞死亡释放的肿瘤抗原可以增强免疫反应;因此,化疗与免疫治疗的联合可能具有协同抗肿瘤效应。许多正在进行的试验,包括CheckMate 77T(纳武利尤单抗)、Impower 030(阿特珠单抗)和Aegean(度伐利尤单抗),正在研究Ⅱ至ⅡB期NSCLC的围手术期免疫治疗-化疗联合方案,这表明该人群的治疗可能从新辅助治疗转向围手术期系统治疗。在KEYNOTE-671中,新辅助帕博利珠单抗联合化疗和辅助帕博利珠单抗单药治疗与安慰剂联合化疗相比,显著改善了EFS和OS,并且病理完全缓解率和主要病理缓解率更高。在CheckMate 77T试验中接受新辅助纳武利尤单抗联合化疗后辅助纳武利尤单抗治疗的患者,以及在Aegean试验中接受新辅助度伐利尤单抗联合化疗后辅助度伐利尤单抗治疗的患者中,也观察到了EFS获益。 本研究存在一些局限性。首先,SEER-Medicare数据库仅包括Medicare保险患者(即≥65岁),因此本研究结果可能无法反映年轻患者人群的结果。然而,在美国,2015年至2019年之间,超过70%的肺癌患者在65岁或以上被诊断,中位诊断年龄为71岁。其次,由于本研究使用的是2007年至2019年的数据(在美国新辅助免疫治疗获批之前),分析仅限于接受新辅助化疗和化疗放疗的患者。第三,由于行政索赔数据的性质,无法直接识别NSCLC复发,因此使用的算法依赖于各种程序、诊断和药物编码,并采用了一定的假设。编码不准确可能导致错分偏倚和NSCLC复发患者的误识别。未在复发时接受治疗或索赔中未记录与转移相关的编码的患者也被遗漏。第四,一些临床信息(如手术结果,即切除状态是否完全)在数据中不可用。因此,使用90天间隔来表示初始治疗的结束,并作为无病状态的代理。第五,尽管本研究使用的数据库能够提供SEER患者的长期结果,但要求在整个研究期间都是Medicare受益人排除了许多SEER人群,导致样本量较小。更多具有较大样本量的真实世界研究可以为可切除NSCLC患者的治疗模式和结果提供更深入的见解。最后,SEER数据缺乏一些肺癌特定的细节,并且不包括治疗设施类型、淋巴结分期方法、化疗周期数或对诱导治疗的病理反应等信息。未来使用包含这些信息的数据库的研究可能是必要的。

编者
本研究为真实世界研究,生存结果可靠可信,新辅助治疗联合手术患者术后总OS为44%,术后的局部区域复发仍是治疗失败的主要原因。

比关注胸外科学苑,共同学习,共同进步

号主:小贾变老贾
|