马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
诊断相关: 共识1:NSCLC LM的诊断应基于临床症状和体征、MRI增强影像和CSF细胞学进行综合诊断,并以细胞学为主要判断依据(A)。 共识2:针对增强MRI和CSF细胞学均阴性但临床仍怀疑LM的患者,可推荐氨基酸类示踪剂PET检查进行补充(B)。 共识3:NSCLC LM患者CSF细胞学采样和诊断流程应遵循多重采样、及时处理的原则(C)。 共识4:CSF ctDNA可以用于明确NSCLC LM患者的驱动基因突变类型和疗效评估(A)。 共识5:CSF CTC检测可作为CSF细胞学阴性并怀疑LM患者的辅助诊断(B)。
治疗原则: 靶向治疗: 共识8:EGFR突变阳性NSCLC患者合并LM,一线治疗优选高CNS渗透性的TKIs,如奥希替尼(A)、伏美替尼等(A),必要时也可考虑佐利替尼(A)。 共识9:对于正在使用EGFR-TKIs靶向治疗的NSCLC患者,如全身症状控制良好但仅新发LM进展时,可以考虑增加原靶向药物的剂量(C)。
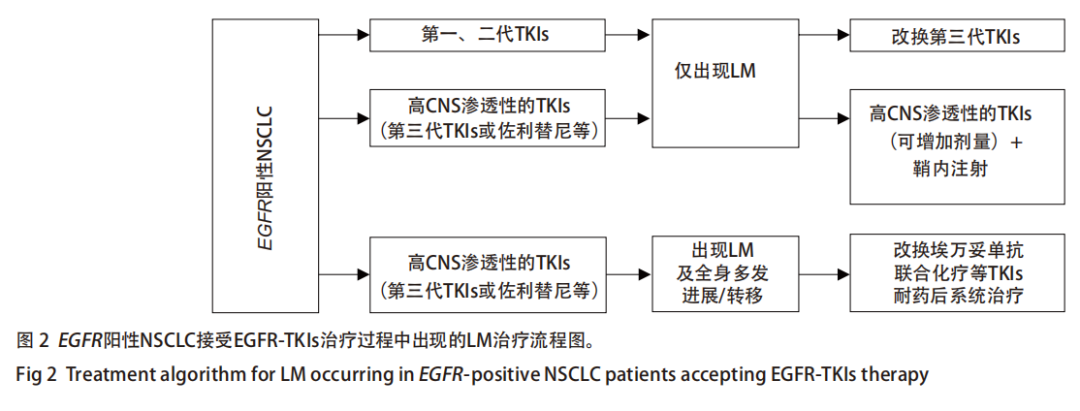
共识10:对ALK阳性的NSCLC LM,应优选洛拉替尼(A)或阿来替尼(B)。
鞘内注射: 放疗: 外科与对症治疗: 共识14:手术切除在已确诊的LM中作用非常有限,一般不推荐。脑膜活检主要用于罕见情况下的完善诊断。如瘤体巨大、局限且症状显著,可行减瘤手术,为后续综合治疗争取时间(A)。 共识15:对于需要鞘内注射的患者,推荐Ommaya囊植入(A)。 共识16:对于颅内压增高症状明显的脑积水患者,应优先考虑脑室腹腔分流或Ommaya囊植入(A)。腰大池腹腔分流可作为交通性脑积水且全麻耐受差患者的治疗替代选择(B)。
放化疗科内容(鞘内注射与放疗)一、鞘内注射治疗:培美曲塞成为新标准
鞘内注射是将药物直接注入蛛网膜下腔,使药物直接接触肿瘤细胞。传统药物如甲氨蝶呤渗透深度有限,疗效受限。本共识明确提出: 优先选择培美曲塞:多项研究显示,培美曲塞鞘内注射在EGFR-TKI耐药后仍能实现较高临床反应率,中位OS可达9–12个月,且耐受性较好。 联合Ommaya囊给药:相比腰椎穿刺,经Ommaya囊脑室内给药能提升药物在脑脊液中的分布均匀性,降低并发症,更适用于需频繁鞘注的患者。 适用时机:主要用于靶向治疗失败或LM进展后的强化治疗,尤其是第三代EGFR-TKI或ALK-TKI治疗期间出现LM进展时。
二、放疗策略:精准与分层的个体化选择
放疗在LM中主要用于缓解症状、控制局部进展,而非根治手段。共识强调: 放疗时机:
放疗方式选择:
局限性病灶:推荐立体定向放射外科/放疗(SRS/SRT),精准打击,保护正常脑组织。 广泛性病灶或症状明显:可考虑全脑放疗(WBRT)或全脑全脊髓放疗(CSI),但需严格评估神经毒性。 质子放疗:质子CSI在研究中显示出潜在优势,但因设备稀缺,暂不作为常规推荐。
本专家共识旨在为相关领域的肿瘤专科医师提供临床决策参考,仅适用于驱动基因阳性的NSCLC患者所发生的LM。文中观点与建议系基于既有证据和专家经验形成,不应被视为绝对正确的结论,亦不构成固定不变的标准治疗方案或临床实践规范,更不能替代临床专科医生在具体情境中的独立判断。本共识所依据的研究证据主要来源于截至2025年10月前收录于PubMed及相关书籍的文献,因而可能无法完全反映其后出现的最新循证进展
中国医药教育协会肺癌医学教育专业委员会, 北京医学奖励基金会肺癌医学青年专家委员会转移性肺癌协作组. 驱动基因阳性非小细胞肺癌脑膜转移临床诊疗中国专家共识(2026版). 中国肺癌杂志, 2026, 29(1): 1–14.
|